マスタープロトコルに基づくがん臨床試験とは?次世代臨床試験デザインの全貌と課題
記事の目次
Toggleはじめに
近年、次世代シークエンサー(NGS)や包括的ゲノム診断パネルの普及により、腫瘍を分子レベルで詳細に分類することが可能になりました。例えば肺癌や乳癌といった従来の臓器別分類に加え、EGFR変異陽性非小細胞肺癌やHER2陽性乳癌といった分子サブタイプが臨床試験の対象となっています。
しかし、患者集団を分子サブタイプごとに細分化すると、希少な部分集団(希少フラクション)が多数生じます。その一つひとつに対して第Ⅰ相から第Ⅲ相試験までを個別に実施することは、研究開発費や時間の観点から現実的ではありません。さらに、試験ごとに異なるプラットフォーム(分子マーカー測定法、患者選定・追跡方法、データマネジメントシステムなど)を用いると、試験間のデータ統合解析において異質性への対応が必要となり、効率性が損なわれます。
この課題を解決するために登場したのが「マスタープロトコル試験」です。共通の基盤システムを用いて複数のサブ試験を並行実施することで、
- 患者間の分子特性の異質性を同一条件下で評価できる
- ゲノムデータの測定精度を均質化し、ドライバー遺伝子変異やシグナル伝達経路の解析が可能になる
- 複数の分子マーカーと標的治療の組み合わせを効率的に探索できる
といった利点があります。
本稿では、がん薬物治療の変遷と分子マーカーを利用した臨床試験デザインの観点から、マスタープロトコル試験が提唱されるに至った背景を整理します。さらに、バスケット試験・アンブレラ試験・プラットフォーム試験の定義と特徴を解説し、国内外の事例を紹介します。最後に、統計的課題や新たに提案されているデザインについても概説し、今後の展望を述べます。
がん薬物療法の変遷とバイオマーカー試験デザイン
がん治療は以下のように進化してきました。
- 従来:細胞障害性薬剤(化学療法)
- 2000年代以降:分子標的薬(例:EGFR阻害薬、ALK阻害薬)
- 近年:免疫チェックポイント阻害薬(例:ニボルマブ、ペムブロリズマブ)
この流れに伴い、臨床試験デザインも進化しました。代表的なのが強化デザイン(enrichment design)です。これは特定の分子マーカー陽性患者のみを対象に薬剤効果を検証する方法です。
例えば、HER2陽性乳癌に対するトラスツズマブ試験(Slamon et al., 2001)は典型例です。
一方、分子マーカーが確立していない場合はマーカー層別デザインが用いられます。陽性群と陰性群に分けてランダム化し、それぞれで効果を検証する方法です。
マスタープロトコル試験の定義と特徴
マスタープロトコル:複数の仮説を同時に検証する包括的プロトコル
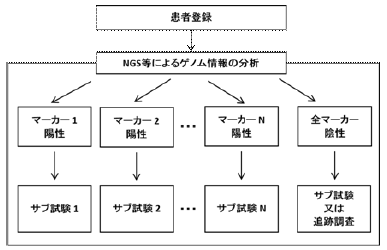
例えば、
- マーカーA陽性 → サブ試験Aへ
- マーカーB陽性 → サブ試験Bへ
- 全て陰性 → 追跡調査へ
このように、共通の基盤システム(検体解析・データ管理・患者選定)を用いることで効率化が図られます。
マスタープロトコルの分類
バスケット試験
定義:複数のがん種に対して、共通の分子マーカーを標的とする薬剤の効果を検証
例:BRAF V600変異を有する複数がん種に対するベムラフェニブ試験
特徴:希少がんや希少フラクションを効率的に登録可能
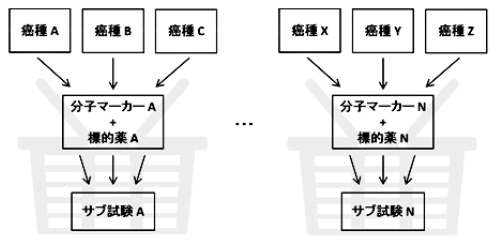
特徴:特定の分子マーカーや遺伝子変異を有する複数のがん種に対して,それに対応する分子標的薬の治療効果をがん種別またはがん種横断的に評価することができます。
アンブレラ試験
定義:単一のがん種に対して、分子マーカー別に複数の薬剤を評価
例:肺腺癌を対象としたALCHEMIST試験(EGFR阻害薬、ALK阻害薬、免疫薬を並行評価)
特徴:検証的試験が多く、標準治療の変化に伴う課題あり
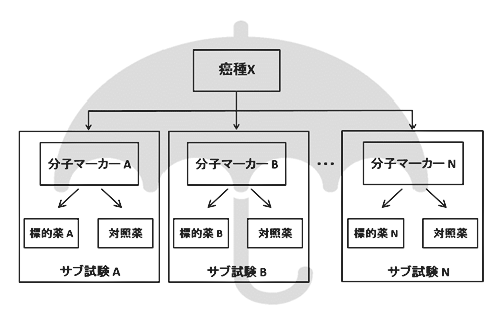
特徴:特定のがん種を対象にして,分子マーカーや遺伝子変異の別に基づいて,それぞれ対応する標的治療を評価するサブ試験を実施します。
プラットフォーム試験
定義:単一疾患に対して複数治療を永続的に評価し、新規治療の追加・除外を許容
例:FOCUS4試験(大腸癌)、I-SPY2試験(乳癌)
特徴:ベイズ統計を用いた中間解析が多く、柔軟性が高い
統計的課題
マスタープロトコル試験は効率的ですが、統計的課題も存在します。
多重性の問題
サブ試験が多数並行すると、第一種過誤率(Type I error)が増大します。
\[P(\mathrm{少なくとも1つの誤検出})=1-(1-\alpha )^k\]
ここで、
- \(\alpha\) :各試験の有意水準
- k:サブ試験数
例えば、\(\alpha =0.05, k=20\)なら、誤検出確率は約64%に達します。
異質性の問題
- バスケット試験ではがん種ごとの予後が異なるため、PFSやOSの比較が困難
- 腫瘍縮小率(ORR)が主要評価項目となることが多い
ベイズ流アプローチ
プラットフォーム試験では、ベイズ推定を用いて中間解析を行い、治療群の追加・除外を柔軟に判断します。
\[Posterior\propto Likelihood\times Prior\]
この枠組みにより、有効性の早期判定や無益性の迅速除外が可能になります。
代表的事例
B2225試験:イマチニブを40種のがんで評価(バスケット試験)
NCI-MATCH試験:遺伝子変異別に30治療を並行評価(バスケット+アンブレラ)
ALCHEMIST試験:肺腺癌に対するEGFR/ALK/免疫薬(アンブレラ試験)
FOCUS4試験:大腸癌に対する複数標的薬(プラットフォーム試験)
I-SPY2試験:乳癌に対するアダプティブデザイン(プラットフォーム試験)
日本における展開
本邦でもマスタープロトコル試験が導入されつつあります。PMDAや厚労省も国際的動向を踏まえ、効率的な臨床試験の枠組みを模索しています。特に希少がんや希少変異に対する薬剤開発において、マスタープロトコルは有力な選択肢となるでしょう。
まとめ
マスタープロトコル試験は、がん臨床試験の効率化と精度向上を目指す次世代の試験デザインです。従来の臓器別・サブタイプ別試験では、患者集団が細分化されることで試験数が膨大になり、費用や時間の面で非現実的でした。これに対し、共通の基盤システムを用いて複数のサブ試験を並行実施するマスタープロトコルは、希少フラクションの患者を効率的に登録し、分子特性の異質性を同一条件下で評価できるという大きな利点を持ちます。
その代表的な形態には、複数がん種に対して単一薬剤を評価するバスケット試験、単一がん種に対して複数薬剤を評価するアンブレラ試験、そして永続的に新規治療を追加・除外できるプラットフォーム試験があります。これらはそれぞれ探索的・検証的な目的に応じて活用され、国際的にも多くの事例が報告されています。
一方で、サブ試験の多重性による第一種過誤率の増大や、患者集団の異質性による評価困難といった統計的課題も存在します。その克服には、ベイズ統計や適応的デザインの導入が不可欠です。
日本でも導入が進みつつあるマスタープロトコル試験は、希少がんや希少変異を対象とした薬剤開発において特に有効であり、規制当局・製薬企業・アカデミアの連携によって今後さらに発展していくことが期待されます。
すなわち、マスタープロトコル試験は「がん臨床試験の新しい標準」となり得る枠組みであり、効率性と科学的妥当性を両立させる次世代の試験デザインとして、今後の臨床研究の中心的役割を担っていくでしょう。
参考
マスタープロトコルに基づくがん臨床試験(2019:平川)
https://www.jstage.jst.go.jp/article/jjb/39/2/39_85/_article/-char/ja