中間解析入門:臨床試験における役割と目的

記事の目次
Toggleはじめに
臨床試験は、新しい薬や治療法の有効性と安全性を科学的に検証するために欠かせないプロセスです。しかし、臨床試験はしばしば数年単位の長期にわたり、多くの患者を対象に行われます。そのため、試験の途中で「この治療は本当に効果がありそうか」「安全性に問題はないか」といった問いに答える仕組みが必要になります。そこで登場するのが中間解析(interim analysis)です。
中間解析とは、臨床試験の最終結果が出る前に、途中段階でデータを解析し、試験の継続可否や方向性を判断するための手法です。本記事では、中間解析の基本的な考え方、目的、具体例を交えながら、なじみのない方にも理解しやすい形で紹介します。
中間解析とは何か
中間解析は、臨床試験の途中で事前に定められたタイミングで行われる統計的解析です。最終的な結論を出すためのものではなく、試験の進行状況を確認し、必要に応じて試験を修正・中止するための判断材料を提供します。
事前に計画される:試験開始前に「いつ」「どのような基準で」中間解析を行うかを治験実施計画書に明記します。
統計的厳密さが必要:途中で解析を行うと「有意差が偶然見えてしまう」リスクが高まるため、統計的な補正(例:有意水準αの調整)が不可欠です。
独立性の確保:解析は通常、独立したデータモニタリング委員会(DMC)が行い、研究者自身は結果を知らないようにすることでバイアスを防ぎます。
中間解析を行う目的
中間解析には大きく分けて以下の目的があります。
安全性の確認
新しい薬や治療法は、予期せぬ副作用を引き起こす可能性があります。中間解析では、重篤な有害事象が多発していないかを確認し、患者の安全を守るために試験を中止する判断が下されることがあります。
有効性の早期確認
場合によっては、治療効果が非常に明確に現れることがあります。このような場合、中間解析で「十分な有効性が確認された」と判断されれば、試験を早期終了し、治療を患者に速やかに届けることができます。これを「早期打ち切りによる成功」と呼びます。
無益性(futility)の判断
逆に、効果がほとんど見られない場合には「このまま試験を続けても有効性は示されない」と判断されることがあります。これを「無益性解析」と呼び、不要な試験継続による患者負担や資源の浪費を防ぐ役割を果たします。
簡単な具体例
ここで、架空の臨床試験を例に考えてみます。
例:新しい抗がん剤の臨床試験
ある製薬会社が新しい抗がん剤を開発し、標準治療と比較する臨床試験を計画しました。対象は200人の患者で、半分が新薬、半分が標準治療を受けます。
- 中間解析のタイミング:100人分のデータが集まった時点で実施。
- 安全性の確認:新薬群で重篤な副作用が標準治療群より明らかに多ければ、試験は中止。
- 有効性の確認:新薬群で腫瘍縮小率が標準治療群より大幅に高ければ、試験を早期終了。
- 無益性の判断:新薬群で効果がほとんど見られなければ、試験を打ち切り。
このように、中間解析は「患者を守る」「資源を有効活用する」「有望な治療を早く届ける」という三つの目的を同時に果たします。
中間解析の意思決定フローを図式化すると以下のようになります。
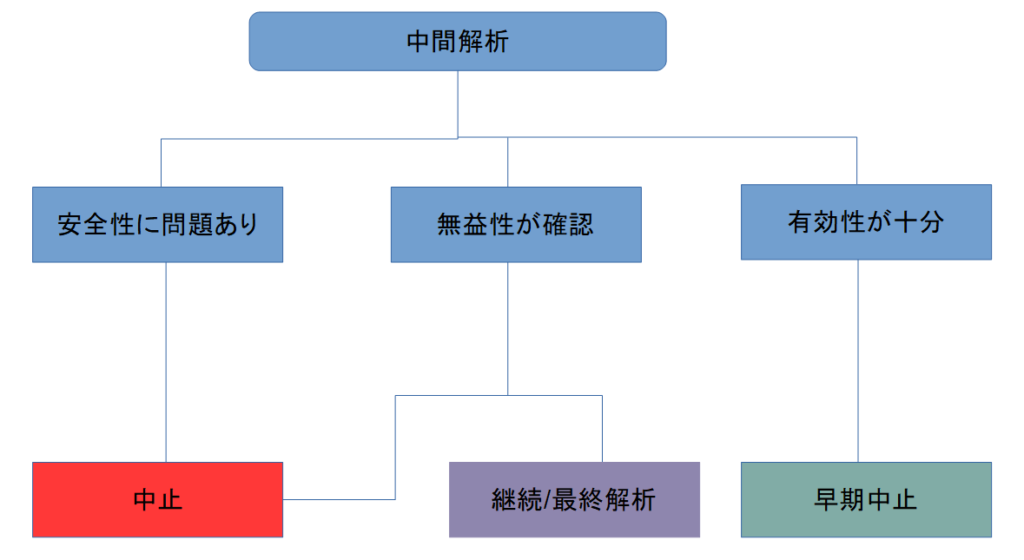
統計的な工夫
中間解析を行うと「偶然の有意差」を拾うリスクが高まります。そのため、中間解析を行う際には、統計的な工夫が不可欠です。代表的な方法として以下があります。
- O’Brien-Fleming法:初期の解析では厳しい基準を設け、後半になるほど緩やかにする方法。
- Pocock法:各解析で同じ基準を用いる方法。
- 有意水準αの調整:複数回解析を行うことで「偶然の有意差」を拾うリスクを減らすため、全体の有意水準を分割して使います。
これらの方法により、中間解析を行っても試験全体の信頼性が損なわれないように設計されています。
例:O’Brien-Fleming法の有意水準(2回解析の場合)
| 解析タイミング | 有意水準 (片側) |
| 中間解析 | 0.005 |
| 最終解析 | 0.048 |
このように、早期の解析では非常に厳しい基準を設け、偶然の有意差を防ぎます。
まとめ
中間解析は臨床試験の途中で安全性や有効性を確認し、試験の継続可否を判断するための重要な仕組みです。統計的補正や独立委員会の存在により、科学的に正当化され、臨床試験の質を高めます。
- 倫理的意義:患者を不利益から守る
- 社会的意義:有効な薬を早く届ける
- 科学的意義:試験の信頼性を保ちながら柔軟に対応
実務では、O’Brien-Fleming法やPocock法などの統計的手法を用い、Rなどのソフトで境界値を計算し、独立委員会が判断を下します。中間解析は、臨床試験の倫理性・効率性・科学性を支える不可欠なツールなのです。