FDAガイダンスを踏まえたランダム化比較試験の共変量調整(導入)

記事の目次
Toggleはじめに
ランダム化比較試験(RCT)における共変量調整(covariate adjustment)は、古くから議論されてきた重要テーマです。特に2023年にFDAが発出したガイダンス
“Adjusting for Covariates in Randomized Clinical Trials for Drugs and Biological Products”は、従来のICH E9やEMAガイドラインの考え方を踏まえつつ、最新の統計理論を反映した内容となっています。
本記事では、日本製薬工業協会データサイエンス部会が作成した報告書「FDAガイダンスを踏まえたランダム化比較試験の共変量調整」1章(背景・目的)と2章(ガイドライン概説)を中心に、共変量調整の基本的な考え方と、各ガイドラインが何を推奨しているのかをわかりやすく整理します。
なぜ共変量調整が重要なのか(1章の要点)
● RCTでも共変量の不均衡は起こる
ランダム化により群間の共変量分布は「平均的には」均衡します。しかし、特にサンプルサイズが小さい試験では、偶然に不均衡が生じることがあります。
このとき、アウトカムと強く関連する共変量が偏ると、以下の問題が起こります:
- 推定精度の低下(統計的効率の低下)
- 条件付きバイアス(conditional bias)の発生
● 共変量調整の目的は「統計的効率の向上」
FDAガイダンスは、共変量調整の主目的を統計的効率(statistical efficiency)の向上と明確に述べています。
統計的効率が上がると以下のメリットがあります。
- 検出力が上がる
- 必要症例数が減る
- 試験成功確率が上がる
● FDAガイダンスの特徴的なポイント(1章より)
FDAガイダンスの特徴として以下が挙げられています:
- 二値アウトカムの条件なし治療効果の推定方法を例示
→ 実務的に新しいアプローチ - 線形モデルで治療×共変量の交互作用を含める方法を議論
→ 従来の「交互作用は入れない」が見直されつつある - モデル誤特定(model misspecification)への強い意識
→ モデルが間違っていても妥当な推論ができる方法を推奨 - 非線形モデルでは estimand の明確化を強調
→ 条件付き治療効果か、条件なし治療効果かを明確に
ガイドライン比較で理解する共変量調整の基本(2章の要点)
2章では、ICH E9、ICH E9(R1)、EMAガイドライン、FDAガイダンスの共変量調整に関する記載が整理されています。
ここでは、実務で重要なポイントに絞って解説します。
ICH E9:共変量調整の基本原則
ICH E9の5.7節には、共変量調整に関する古典的な考え方が示されています。
● 調整すべき共変量は「事前に重要とわかっているもの」
「主要変数に重要な影響を及ぼすと予想される共変量は、試験開始前に議論して確認しておくべき」
● 層別ランダム化をしたら層別因子で調整すべき
「層別因子は解析時に考慮することが適切」
● ランダム化後に測定された変数は調整すべきでない
治療の影響を受けている可能性があるため。
● 交互作用は探索的に扱う
「交互作用解析は探索的であることを明確にすべき」
ICH E9(R1):estimand の考え方が共変量調整に影響する
FDAガイダンスはICH E9(R1)のestimandフレームワークを強く意識しています。
- 治療
- 対象集団
- 変数(評価項目)
- 集団レベルの要約(=治療効果の定義)
共変量調整はこの「集団レベルの要約」に関わるため、estimand を明確にしないと、どの推定量(estimator)を使うべきか決まらないという構造になっています。
estimand と estimator の関係は以下のよう表されます。
\[\mathrm{試験目的}\rightarrow \mathrm{Estimand}\rightarrow \mathrm{推定量(Estimator)}\rightarrow \mathrm{推定値}\]
この流れを明確にすることで、「何を推定したいのか」、「どの推定方法が適切か」が整理されます。
EMAガイドライン:実務的な推奨が中心
EMAガイドラインは、実務での共変量調整の判断基準を明確に示しています。
● 調整すべき共変量の基準
- アウトカムと強い(または中程度の)関連がある
- 臨床的に関連が強いと考えられる
- 層別因子
● 調整すべきでないもの
- 試験後に観察されたベースライン不均衡
→ これを理由に共変量を追加するのはNG - ランダム化後に測定された変数
● ベースライン値がある場合は必ず調整
- 連続アウトカムでは、ベースライン値を共変量に含めることが推奨されます。
● 共変量の数は少数にすべき
- 過剰な調整は過学習や不安定性を招くため。
FDAガイダンス:最新の統計理論を反映したアプローチ
FDAガイダンスは、従来のガイドラインよりも踏み込んだ内容を含みます。
● 特徴1:交互作用を含める線形モデルを議論
- 従来の「交互作用は入れない」が見直されつつあります。
● 特徴2:モデル誤特定への強い意識
- モデルが間違っていても平均治療効果(ATE)を正しく推定できる方法を推奨。
● 特徴3:非線形モデルでは estimand を明確化
- ロジスティック回帰などでは、
- 条件付き治療効果(conditional)
- 条件なし治療効果(marginal)の違いが重要。
● 特徴4:二値アウトカムの条件なし治療効果の推定方法を例示
- 実務で使える具体的手法が示されている点は大きな進歩です。
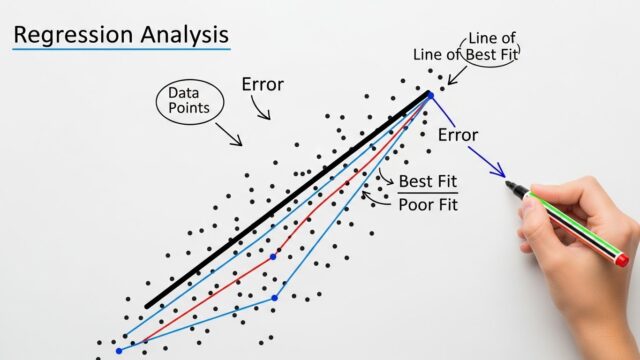
共変量調整の直感的理解
共変量調整の基本モデルであるANCOVAを用いて共変量調整の具体例を示します。
\[Y_i=\beta _0+\beta _1T_i+\gamma X_i+\varepsilon _i\]
- \(Y_i\):アウトカム
- \(T_i\):治療(0/1)
- \(X_i\):ベースライン共変量
- \(\beta _1\):治療効果(推定したい量)
共変量 \(X_i\) を入れることで、誤差分散が減り、推定精度が上がります。
まとめ
本報告書の1章では、ランダム化比較試験におけるベースライン共変量の調整解析が、古くから重要な検討事項であることが示されています。従来はICH E9やEMAガイドラインが主に参照されてきましたが、2023年にFDAが新たなガイダンスを発出したことで、共変量調整に関する考え方が大きく前進しました。FDAガイダンスは、統計的効率の向上を中心テーマとし、治療効果推定の精度向上や検出力の改善、さらには必要症例数の削減につながる点を強調しています。
特に特徴的なのは、線形モデルにおける治療×共変量の交互作用の扱いや、モデル誤特定(model misspecification)を前提とした推定方法への言及が多いことです。また、非線形モデルでは、条件付き治療効果(conditional)と条件なし治療効果(marginal)のどちらをestimandとして定義するかを明確にすべきと述べられており、estimandの考え方が共変量調整と密接に関係することが示されています。
2章では、ICH E9、ICH E9(R1)、EMAガイドライン、FDAガイダンスの共変量調整に関する記載が比較されています。ICH E9では、事前に重要とわかっている共変量の調整や、層別因子の解析への反映が推奨され、交互作用解析は探索的と位置づけられています。ICH E9(R1)では、estimandのフレームワークが導入され、治療効果の定義と推定方法(estimator)を明確に区別することが求められています。EMAガイドラインはより実務的で、アウトカムと強く関連する共変量の調整、ベースライン値の利用、事後的な不均衡を理由に共変量を追加しないことなど、具体的な推奨が示されています。
これらを踏まえると、FDAガイダンスは従来のガイドラインの考え方を包含しつつ、最新の統計理論を取り入れたより実践的で柔軟なアプローチを提示しているといえます。特に、モデル誤特定下でも妥当な推論を可能にする方法や、非線形モデルにおける治療効果の定義の明確化など、今後の臨床試験計画において重要となる視点が多く含まれています。
参考資料
FDAガイダンスを踏まえたランダム化比較試験の共変量調整
(医薬品評価委員会 データサイエンス部会)
https://www.jpma.or.jp/information/evaluation/results/allotment/DS_202506_CovAd.html