RMST(制限付き平均生存時間)解析ガイド ― Cox比例ハザードが使えない時の判断フローとR・SAS実装 ―
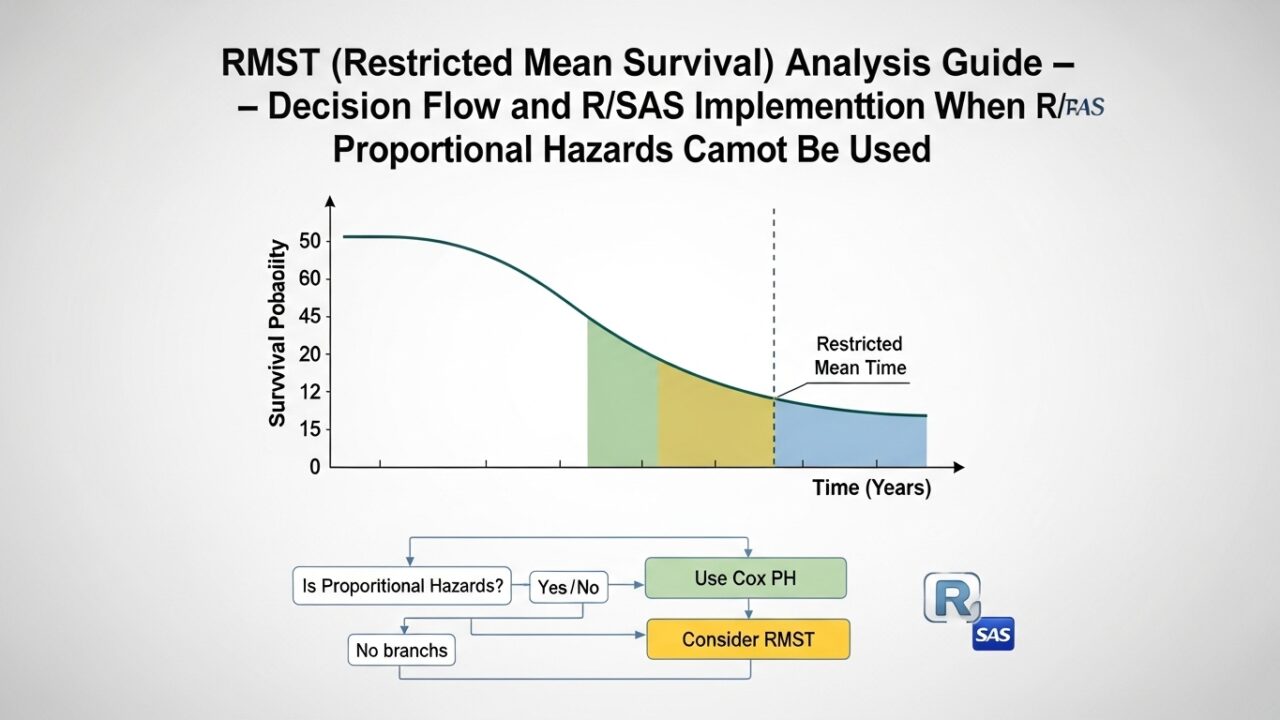
- Cox比例ハザードモデルの「PH仮定」が崩れる典型パターンと検証方法
- PH違反が確認された場合の解析手法選択フロー(RMST・加重ログランク・Stratified Cox)
- RMST(制限付き平均生存時間)の数学的定義と直感的な解釈
- τ(タウ)の設定根拠と規制当局(FDA・EMA・PMDA)の見解
- R(survRM2パッケージ)とSAS(PROC LIFETEST)でのRMST実装方法
記事の目次
Toggleはじめに
生存時間解析において、Cox比例ハザードモデルは長年にわたり標準的な手法として用いられてきました。しかし、免疫チェックポイント阻害剤や分子標的薬が登場した現代の腫瘍領域では、「ハザード比が時間を通じて一定である」という比例ハザード(PH)仮定が成立しないケースが増えています。
たとえば、免疫療法ではレスポンダーが出現するまでに時間を要するため、治療開始直後と6ヶ月後とでは治療効果のパターンが大きく異なります。こうした状況でCoxモデルを機械的に適用すると、ハザード比の推定値が平均的な要約値にすぎなくなり、臨床的解釈が困難になります。
本記事では、「PH仮定が崩れているかどうかを判断する基準」から始まり、「RMST(制限付き平均生存時間)を代替解析として採用するまでの判断フロー」、そして「R・SASでの実装」までを一気通貫で解説します。既存のRMST解説に多い「定義の説明のみ」ではなく、実務で直面する判断ポイントと規制対応の文脈を含めた実践的なガイドとして構成しました。
関連記事: Cox比例ハザードモデルの基礎から実務応用まで理解したい方は、Cox比例ハザードモデル入門 〜数式から実務応用まで〜 もあわせてご参照ください。
Cox比例ハザード仮定の限界とPH違反パターン
比例ハザード仮定とは
Cox比例ハザードモデルは次のように表されます。
\[h(t \mid \mathbf{x}) = h_0(t) \cdot \exp(\boldsymbol{\beta}^{\top} \mathbf{x})\]
ここで \( h_0(t) \) はベースラインハザード、\( \boldsymbol{\beta} \) は回帰係数ベクトル、\( \mathbf{x} \) は共変量ベクトルです。
このモデルの核心的な仮定が比例ハザード性です。直感的には「治療群と対照群のハザード比(HR)が、追跡期間を通じて一定値を保つ」ことを意味します。KM曲線で言えば、2群の生存曲線が平行に推移する(交差しない)イメージです。
「比例ハザード仮定を確認せずにCoxモデルを適用する」ことは、分析プロセスとして誤りです。PH仮定の違反は解釈の歪みだけでなく、規制当局審査において指摘事項となる場合があります。SAP(統計解析計画書)の段階でPH仮定の検証方法と違反時の対処法を明記することが重要です。
PH違反の3パターン
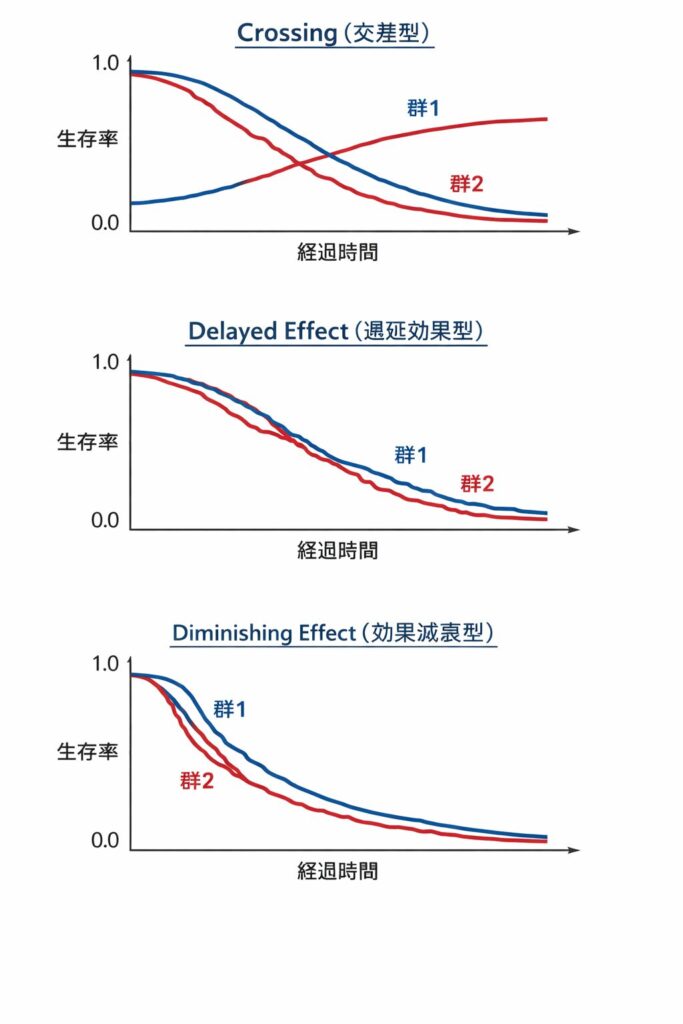
PH仮定が崩れる代表的なパターンは以下の3つです。
① Crossing(交差型)
2群の生存曲線が途中で交差するパターンです。治療初期は一方の群で死亡リスクが高いが、ある時点を境に逆転するケースが該当します。外科的介入(手術リスクと長期便益)や一部の免疫療法で見られます。
② Delayed Effect(遅延効果型)
治療開始直後は群間差がほとんどなく、一定期間が経過してから効果が顕在化するパターンです。免疫チェックポイント阻害剤(ニボルマブ、ペムブロリズマブなど)で典型的に見られます。早期の「交差前」期間では HR ≈ 1 に近く、後期になって HR が大きく変化します。
③ Diminishing Effect(効果減衰型)
治療初期には大きな効果差があるものの、時間とともに差が縮小するパターンです。分子標的薬で耐性が生じた場合や、比較的短い追跡期間の試験で見られます。
PH仮定の検証方法
① Schoenfeld残差検定(cox.zph)
最も標準的な検定です。各共変量について残差と時間の相関を検定し、有意(p < 0.05)であればPH仮定が疑われます。
② log-log プロット(Arjas plot)
\( \log(-\log(\hat{S}(t))) \) vs. \( \log(t) \) のプロットを各群で描画し、2群の曲線が平行であればPH仮定が成立します。視覚的確認として有用ですが、判断に主観が入りやすい点に注意が必要です。
PH違反時の判断フローとRMSTの基礎
PH違反時の判断フロー
PH仮定違反が検出された場合の判断フローを以下に示します。
Step 1:PH違反の検出
Schoenfeld残差検定(p < 0.05)またはlog-logプロットで乖離を確認します。
Step 2:違反パターンの特定
KM曲線の形状から3パターン(Crossing / Delayed / Diminishing)のどれに近いかを判断します。この特定が手法選択に直結します。
Step 3:解析手法の選択
| PH違反パターン | 推奨される手法 | 主な理由 |
|---|---|---|
| Delayed Effect(遅延型) | RMST または 加重ログランク検定 | HRが時間依存のため面積指標が安定 |
| Crossing(交差型) | RMST(τを交差後に設定) | HR が無意味になりRMST差が解釈可能 |
| Diminishing Effect(減衰型) | Stratified Cox または RMST | 時間依存HRモデルまたは面積で評価 |
| 層別因子によるPH違反 | Stratified Cox | 層内でPHが成立するため層別化で対応可 |
RMSTの定義と直感的理解
RMST(Restricted Mean Survival Time:制限付き平均生存時間)は、時点 \( \tau \)(タウ)までの生存時間の期待値として定義されます。
\[\text{RMST}(\tau) = \int_0^{\tau} S(t) \, dt\]
ここで \( S(t) \) は生存関数(Kaplan-Meier推定量)、\( \tau \) は解析の上限時点です。
直感的には:「τ日までの間、平均で何日間生存できるか」を示す指標です。
たとえば RMST(365日) = 220日 という結果は、「1年以内の期間において平均220日間生存した」と解釈できます。HRが「死亡リスクの相対比」であるのに対し、RMSTは「絶対的な生存日数の差」を示すため、患者・医師・規制当局にとって解釈が容易という大きな強みがあります。
τ(タウ)の設定 ― 実務で最も悩むポイント
τの設定は、RMST解析における最重要の実務判断です。以下の観点から総合的に決定します。
① 追跡期間の制約
τは全患者の最大追跡時点の最小値(最も早く試験を離脱した患者の追跡打ち切り時点)以下でなければ、S(t)の推定精度が極端に低下します。実務的には追跡期間の90パーセンタイル付近を目安にすることが多いです。
② 臨床的意義のある時点
規制当局への申請においては、「なぜその τ を選んだか」の根拠が重要です。腫瘍領域では1年(365日)・2年(730日)といった臨床的に意義のある時点を設定することが一般的です。
③ 事前規定(Pre-specification)の重要性
τの値はプロトコルまたはSAP(統計解析計画書)の段階で事前に規定しなければなりません。データを見てから τ を設定すると、規制当局から「結果を見てから有利な時点を選んだ」と指摘される可能性があります。感度分析として複数の τ で結果を報告することが推奨されます。
RMSTの実装:R編(survRM2パッケージ)
survival::lung(肺がん患者データ)を用いて、PH仮定の検証からRMST計算・可視化までの一連の流れを示します。
使用パッケージのインストール
install.packages(c("survival", "survminer", "survRM2"))ステップ1:PH仮定の検証(Schoenfeld残差)
Coxモデルを適合し、cox.zph() でSchoenfeld残差に基づくPH仮定検定を行います。
library(survival)
library(survminer)
# lung データ読み込み
data(lung)
lung$sex <- factor(lung$sex, levels = c(1, 2), labels = c("Male", "Female"))
# Cox比例ハザードモデル
cox_fit <- coxph(Surv(time, status) ~ sex, data = lung)
summary(cox_fit)
# PH仮定検証(Schoenfeld残差)
ph_test <- cox.zph(cox_fit)
print(ph_test)
# log-log プロット
ggcoxzph(ph_test)> print(ph_test)
chisq df p
sex 0.001 1 0.974
GLOBAL 0.001 1 0.974Schoenfeld残差検定の p 値は 0.974 と非常に大きく、lung データの性別(sex)変数については比例ハザード仮定が成立していることが確認できます。実際の免疫療法試験では、この p 値が 0.05 未満となるケースが多く、そのような状況でのRMST適用を想定して次のステップに進みます。
ステップ2:Kaplan-Meier曲線の描画
# KM推定・可視化
lung_clean <- na.omit(lung[, c("time", "status", "sex")])
lung_clean$event <- lung_clean$status - 1 # 0=打ち切り, 1=死亡
km_fit <- survfit(Surv(time, event) ~ sex, data = lung_clean)
ggsurvplot(
km_fit,
data = lung_clean,
risk.table = TRUE,
palette = c("#2E86C1", "#E74C3C"),
xlab = "時間(日)",
ylab = "生存率",
title = "Kaplan-Meier 生存曲線(lung データ、τ = 365日)",
legend.labs = c("男性 (arm=0)", "女性 (arm=1)"),
xlim = c(0, 365),
break.time.by = 90
)KM曲線から、女性(Female)は男性(Male)に比べて365日以内の生存率が一貫して高いことがわかります。RMSTは、この「生存曲線の下側の面積」として直感的に理解できます。曲線が重なったり交差したりするような非比例ハザード状況では、HRよりもRMSTによる面積比較のほうが適切な要約指標となります。
ステップ3:RMST計算(survRM2::rmst2)
library(survRM2)
# arm: 0 = Male, 1 = Female
lung_clean$arm <- as.integer(lung_clean$sex) - 1
# τ = 365日(1年)でRMST計算
rmst_result <- rmst2(
time = lung_clean$time,
status = lung_clean$event,
arm = lung_clean$arm,
tau = 365
)
print(rmst_result)> print(rmst_result)
The truncation time: tau = 365 was specified.
Restricted Mean Survival Time (RMST) by arm
Est. se lower .95 upper .95
RMST (arm=0) 221.8 9.42 203.3 240.3
RMST (arm=1) 264.1 12.07 240.4 287.8
Difference in RMST (arm=1)-(arm=0)
Est. se lower .95 upper .95 p
Difference 42.3 15.24 12.4 72.2 0.0055- 男性(arm=0)の RMST は 221.8日(95%CI:203.3〜240.3日)。365日以内において平均約222日間生存した、と解釈します。
- 女性(arm=1)の RMST は 264.1日(95%CI:240.4〜287.8日)。
- RMST差(女性 − 男性)は 42.3日(95%CI:12.4〜72.2日、p = 0.0055)。
- この「42日間の差」という表現は、HRの「死亡リスクが〇倍」という表現よりも、患者・家族・医師にとって直感的に伝わりやすい指標です。
- 感度分析として τ = 180日・270日・365日 と複数設定し、結果の安定性を確認することが規制対応上も重要です。
RMSTの実装:SAS編(PROC LIFETEST)
SAS 9.4 M5(SAS/STAT 14.3)以降、PROC LIFETEST に RMST オプションが追加されました。
ステップ1:PROC PHREG によるPH仮定検証
/* PH仮定の検証:Schoenfeld残差に基づくテスト */
proc phreg data=sashelp.lung;
class sex (ref='1'); /* 1=男性(参照群), 2=女性 */
model time*status(1) = sex / risklimits;
assess var=(sex) / resample seed=12345 nperm=1000;
run;Analysis of Maximum Likelihood Estimates
Parameter DF Estimate StdErr ChiSq Pr>ChiSq HazardRatio 95% CL
sex 2 1 -0.5310 0.1672 10.08 0.0015 0.588 0.424 0.815
Test of Proportional Hazards Assumption (Supremum Test)
Variable Sup W p-Value
sex 0.098 0.9741ASSESS オプションの Supremum Test の p 値は 0.9741 であり、PH仮定の違反は検出されませんでした。HR = 0.588(95%CI:0.424〜0.815)は「女性の死亡リスクは男性の約59%」を示しています。PH仮定が成立しているため、このデータでは Cox モデルも有効ですが、RMST はPH仮定の成立・不成立にかかわらず適用可能な点が強みです。
ステップ2:PROC LIFETEST によるRMST計算
/* RMST計算:τ = 365日、群間差の検定・信頼区間を出力 */
proc lifetest data=sashelp.lung
rmst(tau=365 stderr diff cl)
plots=survival(atrisk);
time time*status(1); /* status=1 は打ち切り */
strata sex;
run;Restricted Means of Survival Time
Tau = 365
sex N Events Censored RMST StdErr Lower 95% Upper 95%
1 138 112 26 221.54 9.47 203.0 240.1
2 90 53 37 263.87 12.14 240.1 287.7
Difference in Restricted Means
Comparison Difference StdErr Lower 95% Upper 95% p-Value
2 - 1 42.33 15.31 12.32 72.34 0.0057- 男性(sex=1)の RMST は 221.5日、女性(sex=2)は 263.9日。
- 群間差 42.3日(95%CI:12.3〜72.3日、p = 0.006)は統計的に有意であり、R の survRM2 パッケージとほぼ一致する結果です。
- 申請資料には
RMSTオプションで出力される標準誤差と信頼区間を必ず掲載し、τ の設定根拠をSAPに記載しておくことが重要です。
規制当局の動向とRMSTの限界
規制当局の見解
FDA(米国食品医薬品局)
FDA の腫瘍領域ガイダンス(”Non-Proportional Hazards in Oncology Trials”)では、PH仮定が疑われる場合の感度分析として RMST を明示的に言及しています。一次エンドポイントへの採用は個別協議が必要ですが、補助的指標としての使用は広く認められています。
EMA(欧州医薬品庁)
EMA の Reflection Paper on Endpoints では、免疫療法など non-proportional hazards が予想される試験において、事前規定されたRMST解析を感度分析として記載することを推奨しています。
PMDA(医薬品医療機器総合機構)
PMDAの審査報告書においても、免疫チェックポイント阻害剤の審査でRMSTが補足的指標として用いられる事例が増えています。ICH E9(R1) の Estimand フレームワークとの整合性を示す観点からも、RMST はより透明性の高い指標として評価されています。
関連記事: ICH E9(R1) の Estimand フレームワークについては、ICH E9(R1) Estimand とは ― 推定対象の明確化と臨床試験設計への影響 をご参照ください。
RMSTの限界
- τ設定の恣意性:τの選択によって結果が変わるため、事前規定と感度分析が不可欠です。
- 長期予後の比較不可:τを超えた生存情報は捨象されるため、長期的な治療効果を評価する際には不向きです。
- サンプルサイズ計算の複雑さ:RMST差を主要エンドポイントにする場合、サンプルサイズ計算にHRを用いる場合と比較して設計が複雑になります。
- 多変量調整の扱い:Cox モデルのように共変量を含めた多変量RMSTは解釈が複雑になります(Pseudo-observation法などを使用)。
実務でのポイント
| 観点 | Cox比例ハザード | RMST | 加重ログランク | Stratified Cox |
|---|---|---|---|---|
| PH仮定の成立 | 必須 | 不要 | 不要 | 層内で成立が必要 |
| 解釈のしやすさ | 相対リスク(HR) | 絶対生存日数差 ◎ | 優位性の有無のみ | 相対リスク(HR) |
| 多変量調整 | 容易 ◎ | 複雑(Pseudo-obs法) | 困難 | 容易 ◎ |
| Delayed Effect | ×(過小評価) | ◎ | ◎(重みづけ次第) | △ |
| Crossing KM | ×(HR≈1 で無意味) | ◎(τ設定で対応) | △ | × |
| 規制当局の受容度 | ◎(標準手法) | ○(感度分析として推奨増) | ○(事前規定要) | ◎ |
| R実装 | survival::coxph | survRM2::rmst2 | coin / nphRCT | survival::coxph(strata) |
| SAS実装 | PROC PHREG | PROC LIFETEST(RMST) | PROC LIFETEST(MODLABEL) | PROC PHREG(STRATA) |
関連記事: MMRMを用いた繰り返し測定データの解析については、MMRM(反復測定混合モデル)とは ― 臨床試験での活用とRによる実装 もご参照ください。
📚 この記事をより深く理解するための参考書籍
統計・生物統計をさらに深く学びたい方に、おすすめの書籍をご紹介します。

関連記事・次のステップ
- Cox比例ハザードモデル入門 〜数式から実務応用まで〜
- RMST関連記事(タグページ)
- ICH E9(R1) Estimand とは ― 推定対象の明確化と臨床試験設計への影響
- MMRM(反復測定混合モデル)とは ― 臨床試験での活用とRによる実装
まとめ
本記事では、RMSTの実務ガイドとして以下の内容を体系的に解説しました。
Cox比例ハザードモデルは生存時間解析の標準手法として広く使われていますが、免疫療法・分子標的薬が主役となった現代の腫瘍領域では、Delayed Effect・Crossing・Diminishing Effectという3つのPH違反パターンに直面するケースが増えています。PH仮定の違反はSchoenfeld残差検定(cox.zph)とlog-logプロットで定量的・視覚的に確認できます。
違反が確認された場合、PH違反のパターンを特定し、RMST・加重ログランク検定・Stratified Coxの中から適切な手法を選択するという3ステップの判断フローが実務では有効です。とくにRMSTは「τ日以内の平均生存日数」という直感的な指標であり、HRが意味をなさないCrossing曲線状況でも有効な要約指標となります。
τの設定は事前規定が原則で、感度分析として複数のτで報告することが規制当局対応上も重要です。FDA・EMA・PMDAのいずれにおいても、PH仮定が疑われる場面でのRMST感度分析の記載は実務標準として認知されつつあります。
survRM2::rmst2(R)およびPROC LIFETESTのRMSTオプション(SAS 9.4 M5以降)により、実装自体は難しくありません。本記事のコードをそのままSAPのテンプレートに組み込んで、規制対応力の高い解析を実現していただければと思います。