【徹底解説】ICH E10「臨床試験における対照群の選択」

臨床試験の成否を左右する最重要ポイントの一つが、「どの対照群を選ぶか」です。
ICH E10ガイドラインは、この“対照群の選択”に関する国際的な標準的考え方を体系的に整理した文書であり、医薬品開発に携わる研究者にとって必読の内容です。
本記事では、ガイドラインの要点を図解を交えながらわかりやすく解説します。
記事の目次
Toggle対照群を選ぶ理由
臨床試験では、治療効果として観察される変化が
- 薬剤の効果なのか
- 自然経過なのか
- 患者・医師の期待なのか
- 併用療法の影響なのか
を区別する必要があります。
そのために、比較対象(対照群)が不可欠です。
対照群の種類(5タイプ)
ICH E10では、対照群を次の5種類に分類しています。
- プラセボ対照(Placebo)
- 無治療対照(No treatment)
- 用量反応対照(Dose-response)
- 実薬対照(Active control)
- 外部対照(Historical / External control)
それぞれの特徴を簡単に整理します。
プラセボ対照
最も強力に薬効を検出できるデザイン。
ランダム化+二重盲検が基本で、バイアスを最小化できます。
- 有効性を最も明確に示せる
- 絶対的な効果量を測定できる
- 少ない症例数で検出力が高い
- 有効な治療が存在する疾患では倫理的問題
- 患者・医師がプラセボを嫌がり、リクルート困難
無治療対照
プラセボが使えない場合に採用されるが、盲検化できないためバイアスが大きい。
用量反応対照
複数の用量を比較し、用量反応関係を確認するデザイン。
- 有効性と安全性のバランスを評価できる
- プラセボを含めれば薬効の存在を明確に示せる
- 適切な用量設定が難しい
- 用量差が小さいと差が出ないことも
実薬対照(Active control)
既存の標準治療と比較するデザイン。
●目的は2つあります
- 非劣性(equivalence / non-inferiority)を示す
- 優越性(superiority)を示す
●注意点:分析感度(assay sensitivity)
非劣性試験では、「対照薬がその試験条件で確実に効果を示す」ことが前提になります。
外部対照(Historical control)
過去のデータや他施設のデータを対照とする方法。
- 全員に新薬を投与できる
- 希少疾患で有用
- 原則として例外的な状況でのみ使用可能
- バイアスが極めて大きく、信頼性が低い
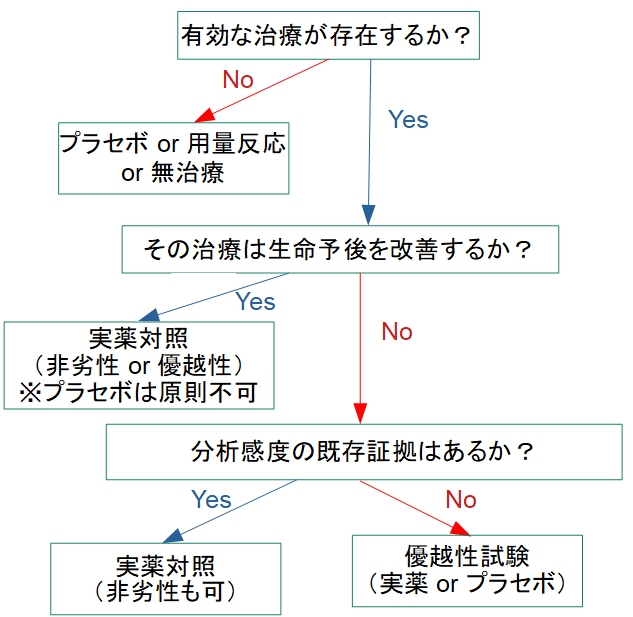
対照群選択の基本ロジック
ICH E10では、対照群選択の考え方を以下のような意思決定ツリーで整理しています。
非劣性試験における「分析感度」の重要性
非劣性試験では、「新薬が対照薬より劣っていない」ことを示します。
しかし、もし試験自体が
- 患者選択が不適切
- 併用薬が多い
- 評価が曖昧
- コンプライアンスが悪い
などの理由で、薬剤間の差を検出できない試験だった場合、
新薬(無効) = 対照薬(有効)
という誤った結論になる危険があります。これが「分析感度」の問題です。
- 過去の試験で対照薬が確実に効果を示しているか確認
- その試験と同様のデザインを採用
- 非劣性マージン(Δ)を妥当な根拠で設定
- 試験を高品質に実施(脱落・併用薬・評価の管理)

プラセボ対照試験の工夫(倫理問題への対応)
プラセボが倫理的に使いにくい場合、ICH E10は以下の工夫を推奨しています。
- 上乗せ試験(Add-on)
→ 標準治療 + 新薬 vs 標準治療 + プラセボ - 置換え試験(Replacement)
→ 標準治療を徐々に減らしながら新薬へ切り替え - 早期離脱デザイン(Early escape)
→ 効果不十分ならすぐ救済治療へ - 短期プラセボ期
→ 試験の最初だけ短期間プラセボを使用 - ランダム化治療中止(Randomized withdrawal)
→ 反応者だけをプラセボ or 継続治療にランダム化
これらにより、倫理性と科学性の両立が可能になります。
外部対照試験の限界と使いどころ
外部対照はバイアスが大きく、原則として推奨されません。
ただし、以下のような例外的状況では有用です。
- 劇的な効果が期待される治療
- 生命を脅かす疾患でランダム化が困難
- 希少疾患で症例が極端に少ない
ただし、使用する場合は
- 患者背景の一致
- 評価方法の一致
- 併用療法の一致
など、厳密な条件が求められます。
まとめ
ICH E10ガイドラインは、臨床試験における対照群選択の基本原則を体系的に示した国際的な基準であり、試験の信頼性を確保するうえで欠かせない指針となっています。対照群の選択は、科学的妥当性、倫理性、そして実施可能性という三つの観点のバランスによって決定されます。プラセボ対照は薬剤の有効性を最も明確に示すことができますが、有効な治療が存在する疾患では倫理的な問題が生じるため、慎重な判断が求められます。一方、実薬対照を用いた非劣性試験では、試験が治療間の差を検出できる能力、すなわち「分析感度」を確保することが極めて重要です。分析感度が不十分な試験では、実際には無効な治療が有効な治療と同等であるかのように見えてしまう危険があり、規制当局に受け入れられない可能性が高くなります。
また、外部対照はバイアスが大きく、原則として例外的な状況でのみ使用されるべきものです。希少疾患や劇的な治療効果が期待される場合など、ランダム化が困難なケースでは有用となり得ますが、患者背景や評価方法の一致など、厳密な条件を満たす必要があります。さらに、プラセボ対照が倫理的に難しい場合には、上乗せ試験、早期離脱デザイン、短期プラセボ期など、倫理性と科学性を両立させるためのデザイン上の工夫が推奨されています。
総じて、ICH E10は、臨床試験の設計において対照群をどのように選択すべきかを判断するための枠組みを提供し、医薬品開発における国際的な整合性と科学的信頼性を支える役割を果たしています。対照群の選択は試験の根幹を成す要素であり、適切な選択と高品質な試験実施が、治療効果の正確な評価と規制当局の承認に直結することをガイドラインは強調しています。