ICH E9(R1) Estimandフレームワーク徹底解説 ― 5属性とintercurrent event戦略の使い分け ―
・ICH E9(R1) Addendumで導入された Estimand(エスティマンド)フレームワークの全体像
・Estimand を構成する 5つの属性(Treatment / Population / Variable / Intercurrent events / Population-level summary)の意味と具体例
・Intercurrent event(中間事象)に対する 5つの戦略の違いと使い分けの判断基準
・糖尿病・オンコロジー・精神疾患など疾患領域別の選択例
・原文(英語)と日本語訳のニュアンスのズレ、PMDA通知や実務での落とし込み方
記事の目次
Toggleはじめに
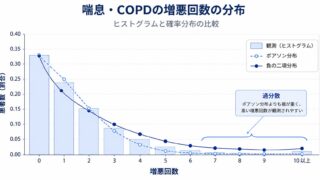
臨床試験の結果を規制当局・医療従事者・患者に正しく伝えるためには、「何を推定しているのか」を曖昧さなく定義する必要があります。従来は ITT(Intention-to-Treat)原則に則っていれば十分とされてきましたが、治療中止・併用禁止薬の投与(rescue medication)・死亡といった intercurrent event(中間事象) をどう扱うかによって、同じデータから導かれる治療効果の解釈は大きく変わります。
この問題意識から ICH は 2019年11月20日に E9(R1) Addendum(Estimands and Sensitivity Analysis in Clinical Trials) を Step 4 として採択し、Estimand フレームワーク を国際調和基準として位置づけました。日本でも厚生労働省から通知が発出され、現在はプロトコル・統計解析計画(SAP)における Estimand の明示が標準となりつつあります。
本記事では、製薬企業の生物統計担当者・臨床開発担当者・CRO・アカデミアの統計家の方が、5属性と5戦略を自分の担当プロトコルに落とし込めるレベルまで理解できるように、具体例と判断基準を体系的に整理します。
Estimand とは ― 「推定すべきもの」の厳密な定義
Estimand(エスティマンド)は、日本語では「推定対象」と訳されます。ICH E9(R1) 原文では以下のように定義されています。
A precise description of the treatment effect reflecting the clinical question posed by a given clinical trial objective.
つまり、試験の目的(clinical question)に対応する治療効果を、誤解の余地なく規定したものです。ここでのポイントは、Estimand が「解析手法」ではなく「推定の対象」そのものであることです。同じ解析手法(例:MMRM)を使っても、Estimand が異なれば結論は別物になります。
従来の枠組みとの違いを整理すると次のようになります。
| 観点 | 従来(ITT中心) | Estimand フレームワーク |
|---|---|---|
| 出発点 | 解析集団・解析手法の議論 | 推定したい治療効果の定義 |
| 中間事象の扱い | 暗黙的・事後対応になりがち | 5戦略から明示的に選択 |
| 欠測との関係 | 欠測と中止が混在 | ICE と欠測を明確に分離 |
| 感度分析の位置づけ | 追加解析として任意 | Estimand に紐づいた必須プロセス |
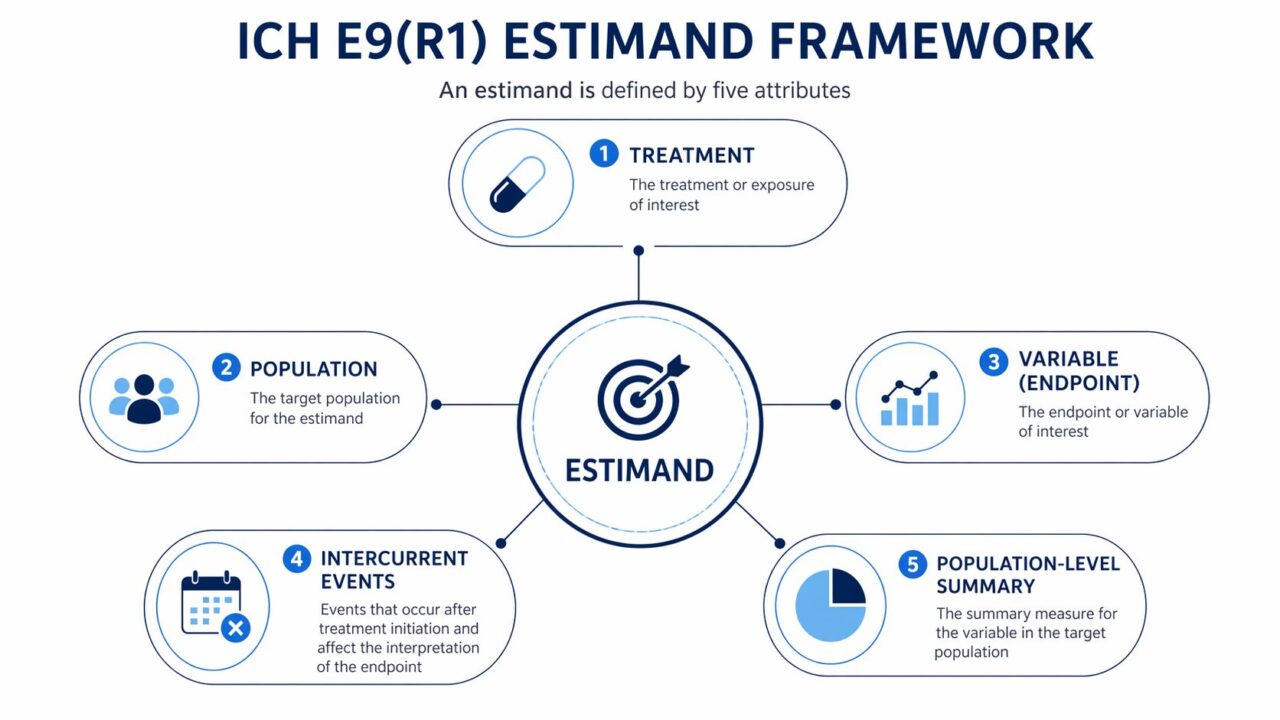
Estimand を規定する5つの属性
Estimand は以下の5属性で一意に規定されます。いずれが欠けても「治療効果の定義」として成立しません。
| # | 属性(英) | 日本語訳 | 内容 |
|---|---|---|---|
| 1 | Treatment | 治療 | 比較したい治療条件と対照。単剤か併用か、投与期間、用量調節ルールまで含む |
| 2 | Population | 対象集団 | 推定対象となる患者集団。選択・除外基準で規定される |
| 3 | Variable (Endpoint) | 評価変数 | 各被験者から得られる評価項目。時点・単位・定義を含む |
| 4 | Intercurrent events | 中間事象 | 治療開始後に生じ、測定値の解釈または取得に影響する事象と、その取り扱い戦略 |
| 5 | Population-level summary | 集団レベルの要約指標 | 治療群間比較に用いる要約統計量(平均差、オッズ比、ハザード比、奏効率差 など) |
Intercurrent event(ICE)は「治療中止」「rescue投与」のような事象そのものを指します。一方、欠測(missing data)はその後「測定値が取れるかどうか」というデータ取得の問題です。ICE が起きても測定は継続可能な場合があり、逆にICEがなくても欠測は生じ得ます。この2つを混同してしまうと、戦略の選択と感度分析の設計を誤ります。
Intercurrent event に対する5つの戦略
ICH E9(R1) は ICE の扱い方として次の5つの戦略を提示しています。どの戦略を選ぶかで、推定される治療効果の臨床的意味が根本的に変わることに注意が必要です。
| 戦略 | 扱い方 | 対応する臨床的問い | 代表例 |
|---|---|---|---|
| Treatment policy 治療方針戦略 | ICEが起きても無関係に、観測された結果を使う | 実臨床での治療方針を割り当てた場合の効果は? | オンコロジーのOS評価 |
| Hypothetical 仮想戦略 | ICEが起きなかったと仮定したシナリオで推定 | ICEが起きなかったら治療効果はどうだったか? | 糖尿病HbA1c(rescue投与なしの効果) |
| Composite 複合戦略 | ICE 自体を失敗・エンドポイントの一部に組み込む | 効果とICE回避を合わせた総合的成功率は? | 精神疾患・治療継続率付き有効率 |
| While on treatment 投与中戦略 | ICE発生前(投与中)のデータのみを使う | 投与されている間の治療効果は? | 症状スコア・QOL(緩和ケア領域) |
| Principal stratum 主要層別化戦略 | 特定の潜在的層(ICEが起きない被験者群)で推定 | ICEが起きない部分集団での効果は? | ワクチン試験(感染後のICU移行など) |
5戦略の選択は、疾患領域・エンドポイント・規制当局の期待値によって変わります。記事末尾の参考書籍では、丹後俊郎『臨床試験ハンドブック ― デザインと統計解析』をはじめ、Estimand を実務プロトコルへ落とし込むための定番書をまとめています。
疾患領域別:どの戦略を選ぶべきか
抽象論で止まると戦略選択は難しいため、代表的な疾患領域で「臨床的問いと戦略の対応」を確認します。
① 糖尿病(HbA1cを主要エンドポイントとする試験)
血糖コントロールが不良となった被験者にレスキュー療法を投与することがあります。レスキュー投与後の HbA1c は本来の治療効果を反映しません。したがって「被験薬本来の効果」を問うなら Hypothetical strategy(レスキュー投与が起きなかったと仮定)が自然です。一方、「実臨床での治療戦略としての有効性」を問うなら Treatment policy、「レスキュー不要で血糖コントロールを維持できた割合」を問うなら Composite となります。
② オンコロジー(OS:全生存期間)
OS はそもそも死亡をイベントとするため、治療中止・後治療(subsequent therapy)が入っても測定は継続可能です。一般に Treatment policy strategy が第一選択となり、規制当局も受け入れやすい設計です。ただし PFS(無増悪生存期間)では後治療の影響をどう切り分けるかが論点となり、Hypothetical の適用も議論されます。
③ 精神疾患(うつ病・統合失調症など)
治療中止率が高く、かつ中止が「効果不十分」と「忍容性」の両方を含むため、単純な Hypothetical は誤解を招きやすい領域です。Composite strategy(「治療継続かつ改善」を成功と定義)や、While on treatment の併用が実務的に増えています。
④ ワクチン・感染症領域
「感染後に治療を受けた群」と「感染しなかった群」は潜在的に異なる集団です。感染しなかった被験者だけを層として効果を推定したい場合は Principal stratum strategy が用いられますが、同定不能性(identifiability)の問題があり、強い仮定と感度分析が必須となります。
原文と日本語訳のニュアンスのズレ
E9(R1) は英語原文で理解するのが最も正確ですが、日本語訳を使う際は次のズレに注意してください。
| 原文 | 日本語訳(通知等) | 注意点 |
|---|---|---|
| Estimand | 推定対象 | 「推定値」ではない点を強調。英語のまま使うのが無難 |
| Intercurrent event | 中間事象 | 「中間解析」との混同に注意 |
| Principal stratum | 主要層別化 | 潜在的サブグループを意味しており、共変量による層別とは異なる |
| Sensitivity analysis | 感度分析 | ICH E9(R1) では「仮定の頑健性確認」に限定される。補助解析とは区別される |
実務でのポイント
1. Estimand を決めてから解析手法を決める:MMRM や multiple imputation は手段であって Estimand ではありません。
2. 主要 Estimand+補助 Estimand を設計:規制当局向けの主要 Estimand と、実臨床解釈向けの補助 Estimand を併記すると説明力が上がります。
3. ICE ごとに戦略を割り当てる:「治療中止」と「rescue投与」に別々の戦略を当てることも可能です。
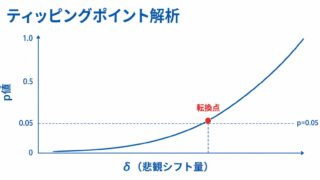
4. 感度分析は Estimand 単位で設計:Hypothetical strategy を選んだ場合の tipping point analysis など、戦略ごとに適切な手法が決まります。
5. PMDA・FDA・EMA 間の期待値の違いを確認:同じ疾患でも地域ごとに推奨が異なる場合があり、事前相談での摺り合わせが有効です。
📚 この記事をより深く理解するための参考書籍
Estimand フレームワーク・臨床試験デザイン・統計解析の実務を深めたい方におすすめの書籍です。



関連記事・次のステップ
- ICHガイドラインシリーズ:ICH E20(臨床試験のためのアダプティブデザイン)とは ― Step 4最終化目前!国際調和ガイドラインの全体像
- 統計手法シリーズ(次回実装で使用):MMRM(反復測定混合モデル)と多重代入法の組み合わせ解析 ― RとSASによる実装ガイド
- 感度分析の深掘り:多重代入法(Multiple Imputation)応用編 ― MNAR感度分析・シミュレーション比較・SAS/Rの深掘り実装
次回は本記事で扱った Estimand を実装する代表的な手法として、MMRM(Mixed-effect Model for Repeated Measures)・multiple imputation・tipping point analysis を R コード付きで解説する予定です。Hypothetical strategy を選択した際の感度分析の実際についても踏み込みます。
まとめ
本記事では、ICH E9(R1) Addendum で導入された Estimand フレームワーク を、5属性(Treatment / Population / Variable / Intercurrent events / Population-level summary)と、intercurrent event に対する5戦略(Treatment policy / Hypothetical / Composite / While on treatment / Principal stratum)という2軸で整理しました。
従来の ITT 原則では曖昧だった「中間事象の扱い」を明示的に決めることで、試験の臨床的問いと統計解析が一直線でつながるようになります。これはプロトコル品質の向上だけでなく、規制当局・医療従事者・患者との対話の質そのものを変える大きな転換点です。
担当中のプロトコルがある方は、ぜひ一度「この試験の Estimand は5属性で書き下ろせるか」「ICE ごとにどの戦略を選んでいるか」を見直していただければと思います。Estimand を正しく定義できることは、これからの生物統計家にとって大きな強みになります。