ベイズ臨床試験デザイン入門 ー FDA 2026年ドラフトガイダンスから読み解く事前分布・予測確率・適応的デザイン ー
・ベイズ流アプローチが臨床試験デザインで注目される理由
・事前分布・尤度・事後分布の3点セットの直感的理解
・過去データを活かす MAP事前分布(RBesT)の使い方
・中間解析を支える「予測確率(PoS)」の考え方
・FDA 2026年ドラフトガイダンスが示す規制側の方向性
記事の目次
Toggleはじめに
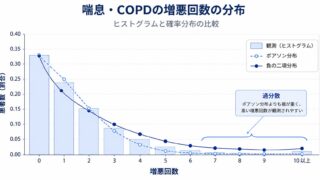
近年、希少疾患や小児領域・FIH(First-in-Human)試験など、被験者数を確保しにくい開発状況が増えています。「すべての試験を頻度論で大規模に検出する」設計が現実的でない場面では、過去データや専門家の知見を確率分布として組み込めるベイズ流アプローチが、合理的かつ実装可能な選択肢として急速に広がっています。
2026年1月にはFDAがドラフトガイダンス『Use of Bayesian Methodology in Clinical Trials of Drug and Biological Products』を公表し、製薬業界における議論が一気に活発になりました。これにより、これまで補助的解析に留まりがちだったベイズ手法が、ピボタル試験の主要評価変数の推論にも明示的に位置づけられ、開発戦略の幅が大きく広がりつつあります。
本記事では、ベイズ臨床試験デザインの根幹である 事前分布・予測確率・適応的デザイン の考え方を、Rパッケージ RBesT の実装例を交えて整理します。製薬業界の生物統計担当者として「ベイズ流デザインを設計選択肢に加えるための最初の一歩」を体系的に押さえていただける構成です。
ベイズ流アプローチの基本:事前分布 × 尤度 = 事後分布
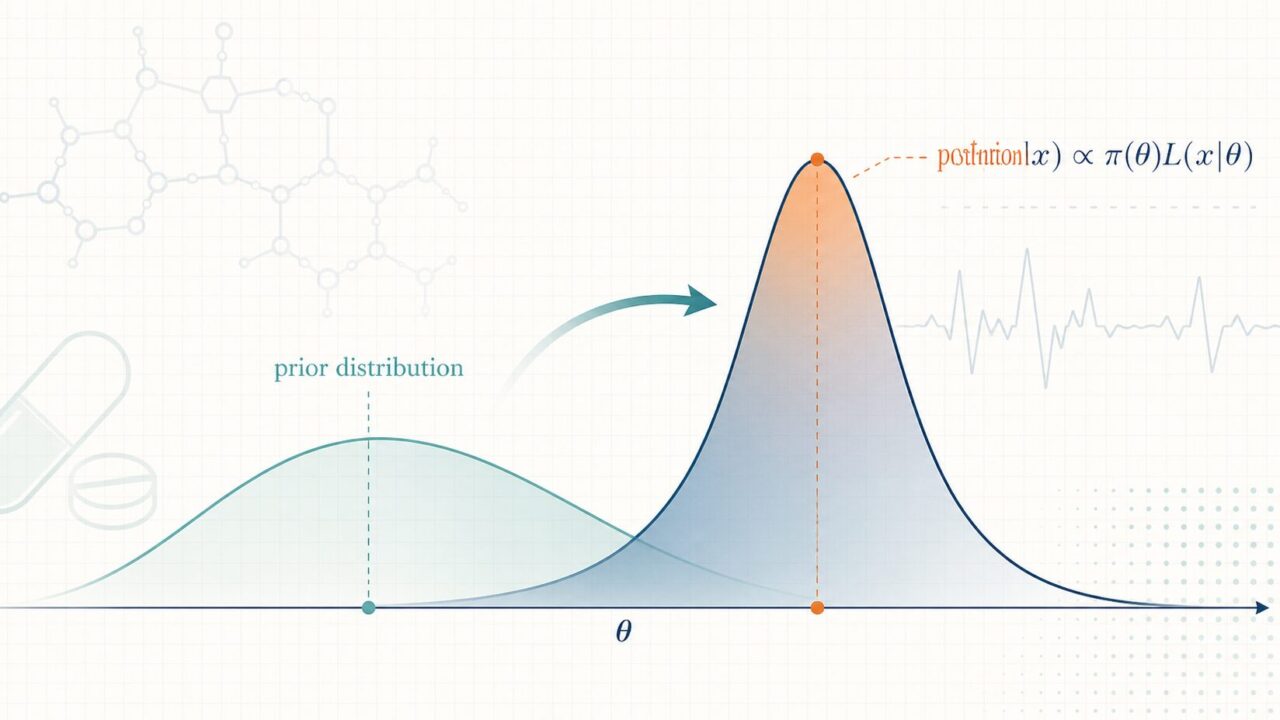
ベイズ統計の出発点は、未知パラメータ θ(例:治療効果や奏効率)を確率変数として扱い、観測前に持っている情報を 事前分布 π(θ) で表現する点にあります。試験から得られたデータ x が与えられた後の分布が 事後分布 π(θ|x) であり、両者は次のベイズの定理で結ばれます。
\[ \pi(\theta \mid x) \;\propto\; \pi(\theta) \;\times\; L(x \mid \theta) \]
ここで \(L(x \mid \theta)\) は尤度関数で、頻度論で扱う「データの確率」と同じものです。重要なのは、頻度論が「データはランダム、θ は固定」と考えるのに対し、ベイズ流は「θ もデータも、どちらも確率的に扱う」点です。
この発想転換により、「θ が一定値以上である確率」「将来の患者で有効である確率」といった、開発判断で本来知りたい確率言明が 直接 得られるようになります。p値や信頼区間に関する誤解(cf. 信頼区間とp値の関係を図解で理解する)に悩まされにくいのは、ベイズ流の大きな実務的利点です。
ベイズ臨床試験デザインの主な活用場面
ベイズ流アプローチは万能ではなく、頻度論より特に強みを発揮する場面があります。下表は代表的な4つの活用場面です。
| 場面 | 概要 | 主なメリット |
|---|---|---|
| FIH/PoC試験 | 用量探索・概念実証 | 小サンプルでも意思決定可能 |
| 希少疾患 | 患者数が限定的な開発 | 過去データを情報源として組込 |
| 適応的デザイン | 中間解析で標本拡張・打切 | 予測確率に基づく go/no-go |
| 外部対照 | 過去対照群でプラセボ縮小 | MAP事前分布で歴史的対照を活用 |
特に 適応的デザイン との親和性は高く、ICH E20(臨床試験のためのアダプティブデザイン) の文脈でもベイズ流の中間判断は標準的な選択肢になっています。
事前分布の選択:MAP事前分布とRBesT
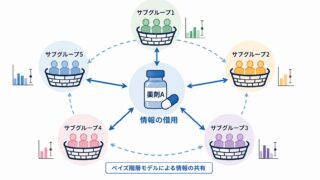
ベイズ臨床試験デザインで最も実務的に使われる事前分布が MAP(Meta-Analytic-Predictive)事前分布 です。複数の過去試験のメタアナリシスから、新試験の対照群パラメータの予測分布を導出し、それを事前分布として用います。
Novartis社が公開する RBesT(R Bayesian evidence synthesis Tools) パッケージは、この MAP 事前分布の構築を Stan ベースで実装した代表的なツールで、CRAN・GitHub から無償で利用できます。次のコード例は、過去6試験の対照群成功例数から MAP 事前分布を構築し、有効サンプルサイズ(ESS)を算出するものです。
library(RBesT)
set.seed(123)
# 過去6試験の対照群(n: 試験規模、r: 成功例数)
hist <- data.frame(
study = paste0("S", 1:6),
n = c(80, 95, 72, 110, 65, 88),
r = c(28, 35, 25, 42, 22, 30)
)
# MAPメタアナリシス(gMAP)→ 混合分布近似(automixfit)
map_mc <- gMAP(cbind(r, n - r) ~ 1 | study,
family = binomial,
data = hist,
tau.dist = "HalfNormal", tau.prior = 1,
beta.prior = 2)
map_prior <- automixfit(map_mc)
# 有効サンプルサイズ
ess(map_prior)> ess(map_prior)
[1] 42得られたMAP事前分布の有効サンプルサイズ(ESS)は約42。新試験で対照群80名を割付ける場合、過去情報の寄与によって実質的に「対照群120名相当」の情報量を得ていることになります。プラセボ群を縮小する設計判断の根拠として、規制当局との議論にもそのまま提示できる定量的な指標です。
予測確率(PoS)と中間意思決定
ベイズ臨床試験デザインのもう1つの核は 予測確率(Probability of Success, PoS) です。中間解析時点までのデータを用いて、「最終解析時に成功する事後予測確率」を計算し、go/no-go 判断に直結させます。
PoS は中間データから事後分布を更新したのち、残りの患者データを将来の観測値としてモンテカルロ的に発生させ、最終解析時点での成功確率を平均化することで得られます。実運用では、計画書段階で以下のような閾値を設定しておくのが一般的です。
| PoS | 推奨アクション |
|---|---|
| ≥ 80% | 加速・標本拡張・早期成功宣言 |
| 50–80% | 計画継続 |
| 20–50% | 注意・継続検討(プロトコル修正) |
| < 20% | 早期中止(無効中止)の検討 |
頻度論の条件付き検出力(conditional power)と比べ、PoS は事前分布で表現された不確実性を含むため、より保守的かつ意思決定者に直感的な指標となります。
ベイズ理論を体系的に押さえるなら『標準ベイズ統計学』、Stan/Rの実装は『RとStanではじめる ベイズ統計モデリングによるデータ分析入門』が定番です。記事末尾でランキング形式に紹介していますので、レベルに合わせて1冊選んでみてください。
規制動向:FDA 2026年ドラフトガイダンス
FDAは2026年1月9日、医薬品・生物学的製剤の臨床試験におけるベイズ手法の活用に関するドラフトガイダンスを公表しました(パブリックコメント締切:2026年3月13日)。要点は以下の通りです。
- 第一義的な推論への適用:これまで補助的解析に限定されがちだったベイズ手法を、主要評価変数の推論にも明示的に許容する方針が示されました。これにより、ベイズ流デザインの規制対応上のハードルが大きく下がります。
- シミュレーション中心の運用特性評価:第I種の過誤率(α)を頻度論的に較正することを基本としつつ、特殊な状況では事前合意のもと、ベイズ流の運用特性指標(例:誤った go/no-go の確率)も認める柔軟性が示されています。
- 外部データ(歴史的対照・RWD)の組み込み:MAP事前分布などを通じた借入を体系的に位置づけ、ESS の透明な提示や事前感度分析を求めています。
ドラフト段階のガイダンスは最終版で記載が変わる可能性があります。実際のプロトコル設計時は最新の確定版を必ず確認し、規制当局との事前相談(Type Cミーティング等)を活用してください。日本国内の場合は PMDA との対面助言も有効です。
実務でのポイント
・事前分布は事前に固定:データを見てから事前分布を変えると規制側の信頼を失います。プロトコル確定時に固定し、感度分析を併設するのが定石です。
・頻度論的較正を残す:FDA ガイダンスもデフォルトはシミュレーションでの第I種過誤率較正を要求しています。完全にベイズ流のみで突き進むケースは限定的と捉えるのが安全です。
・ESS(有効サンプルサイズ)を必ず提示:歴史的対照を組み入れる際は、組み入れ量の透明性を担保する指標として ESS を併記してください。
・Estimand と整合させる:ICH E9(R1) Estimandフレームワーク と矛盾しない事後分布の解釈を構築することが、申請対応上きわめて重要になります。
📚 この記事をより深く理解するための参考書籍
ベイズ統計・臨床試験デザインをさらに深く学びたい方に、おすすめの書籍を3冊ご紹介します。


関連記事・次のステップ
- ベイズ統計の解析手法と製薬業界での活用:本記事と対をなす「解析手法」側のまとめ。R/SASでの実装をより詳しく扱っています。
- ICH E20(臨床試験のためのアダプティブデザイン)とは:適応的デザイン全般の国際調和ガイドライン。ベイズ流意思決定の前提として必読です。
- ICH E9(R1) Estimandフレームワーク徹底解説:事後分布が「何の」確率を表すのかを規律づけるための前提知識として重要です。
まとめ
本記事ではベイズ臨床試験デザインの基礎、すなわち 事前分布・尤度・事後分布の関係 から、MAP事前分布の構築(RBesT)、予測確率(PoS)による意思決定、そして FDA 2026年ドラフトガイダンス までを体系的に整理しました。
ベイズ流アプローチは「使うかどうか」ではなく「どこで・どのように使うか」を設計する時代に入りつつあります。希少疾患・FIH・外部対照を視野に入れる開発では、頻度論一辺倒では実現しにくい合理的な意思決定が可能になり、開発期間の短縮や被験者負担の軽減にも直結します。
次回は、本記事で紹介した RBesT を用いた 歴史的対照データを借入する具体的な実装事例 と、感度分析・運用特性シミュレーションの作り込み方を、より具体的なシナリオで解説します。製薬業界の生物統計担当者として、ベイズ流デザインを設計選択肢に加えていただければと思います。