リアルワールドエビデンス(RWE)入門 ― 規制活用と外部対照群への展開 ―
・リアルワールドデータ(RWD)とリアルワールドエビデンス(RWE)の違い
・FDA・PMDA・EMAがRWEに対して示している規制上の最新スタンス(2024〜2025年動向を含む)
・外部対照群(External Control Arm, ECA)の構築フローと、傾向スコア・MAICなどの統計手法
・RWE活用で必ず押さえるべきバイアスと、製薬実務での具体的注意点
記事の目次
Toggleはじめに
ランダム化比較試験(RCT)は治療効果を評価するうえで最も信頼性が高い設計であり、これからもエビデンスの中心であり続けます。一方で、希少疾患・小児・ライフサイクルの長い領域、あるいは倫理的にプラセボ群が組めない領域では、RCT以外のデータをどう活かすかが大きな論点になっています。ここで主役になるのが、リアルワールドデータ(RWD)とそこから生成されるリアルワールドエビデンス(RWE)です。
製薬企業の生物統計家・メディカル・レギュラトリーの立場では、RWEはもはや「使うかどうか」ではなく「どう設計し、どう規制当局に説明するか」のフェーズに入っています。FDAは2025年12月に医療機器向けRWEガイダンスを最終化し、ICH M14(薬剤疫学)も2024年7月にドラフト公開されるなど、規制側も急速に整備が進みました。本記事では、RWEの基本概念から、外部対照群への活用、統計手法、バイアスまでを実務観点で体系的に整理します。
RWDとRWEの違い ― 用語整理
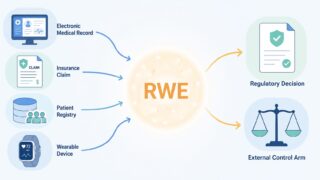
リアルワールドデータ(RWD: Real-World Data) は、診療・保険請求・患者報告など日常診療の現場で収集された、いわば「素材」のデータです。これに対し、リアルワールドエビデンス(RWE: Real-World Evidence) は、RWDを統計解析することで導かれる「治療法の使用法・潜在的なベネフィットや安全性に関する臨床的エビデンス」を指します。
FDAのRWE Frameworkでは、両者をはっきり区別したうえで「RWDをどう加工すれば規制判断に耐えるRWEになるか」という観点で議論しています。素材であるRWDの品質と、解析設計を含めたRWE生成の透明性、その両方が揃ってはじめて承認申請に活用できる、というのが共通認識です。
| 用語 | 中身 | 代表例 |
|---|---|---|
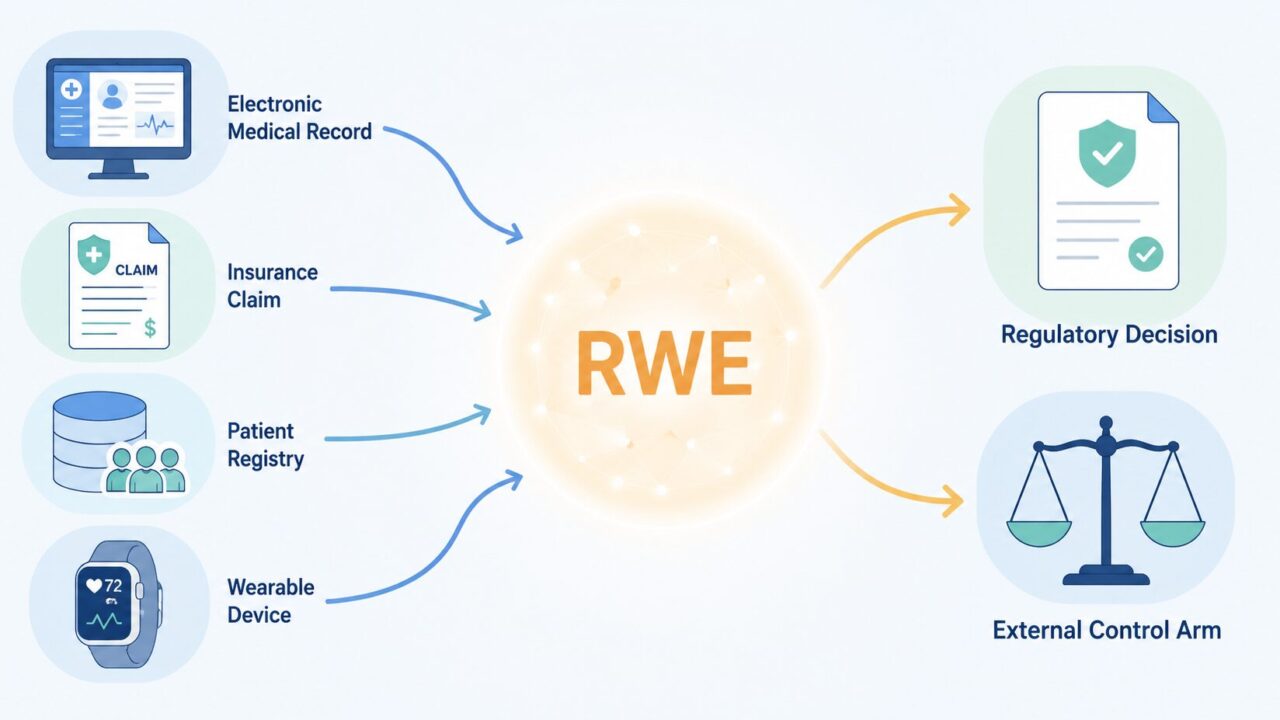
| RWD(素材) | 日常診療で生成される個別データ | 電子カルテ/レセプト/疾患レジストリ/ウェアラブル |
| RWE(成果物) | RWDから統計解析で得られる臨床的知見 | 市販後の有効性・安全性比較/外部対照群との効果比較 |
| RCT | 介入を割り付けた前向き試験 | 第Ⅲ相検証試験/二重盲検プラセボ対照 |
| プラグマティック試験 | RCTとRWEの中間。日常診療下で行うRCT | 電子カルテベースの実臨床ランダム化試験 |
ポイントは「RWE = RWD + 解析方法 + 解釈」という3点セットで成立する、という捉え方です。RWDだけ揃えても規制当局には通らず、解析計画と結果解釈の妥当性を併せて示す必要があります。
規制上の位置づけ ― FDA・PMDA・EMAの最新動向
FDA:医療機器ガイダンスを2025年12月に最終化
FDAは2018年12月に「Framework for FDA’s Real-World Evidence Program」を公表し、新薬・バイオ製品でのRWE活用を本格化させました。その後、2023年8月には「Considerations for the Use of Real-World Data and Real-World Evidence to Support Regulatory Decision-Making for Drug and Biological Products」を最終化し、医薬品領域でのRWD/RWEの判断基準(妥当性・信頼性)を明確にしました。
医療機器領域では、2017年版を全面改訂した「Use of Real-World Evidence to Support Regulatory Decision-Making for Medical Devices」が2025年12月18日に最終化されました。改訂版では、RWDの「relevance(妥当性)」と「reliability(信頼性)」の評価をベネフィット・リスク評価のフレームワークに統合する方針が示されています。さらに、2024年7月にはICH M14(医薬品の安全性評価における薬剤疫学調査の計画・デザイン・解析)のドラフトが公開されており、安全性評価でのRWE活用が国際的に標準化される段階に来ています。
PMDA:RWD WG(2021年4月〜2024年9月)と信頼性ガイダンス
国内では、PMDAが「RWD WG(リアルワールドデータワーキンググループ)」を2021年4月から2024年9月まで設置し、医薬品・医療機器・再生医療等製品のライフサイクルを通じたRWD活用の基本的考え方と信頼性確保策を整理しました。レジストリやデータベースの信頼性に関する考え方を示すガイダンスや事務連絡が複数発出されており、薬事承認審査での実装に向けた準備が進んでいます。
IMDRF:RWDの「6つの視点」
国際医療機器規制当局フォーラム(IMDRF)は、RWDの品質担保のために代表性・完全性・正確性・一貫性・信憑性・信頼性という6視点を提示しました。PMDA・FDAの考え方の根底にもこの整理が流れており、RWE生成計画書(プロトコル)を書く際のチェック項目としてそのまま使えます。
規制当局は「RWEの活用に積極的」と「どんなRWEでも受け入れる」をはっきり区別しています。あくまで 事前協議(PMDA対面助言/FDAミーティング)でデザインの妥当性を共有しておくこと が前提であり、解析後にRWEを後付けで提示しても採用されにくいのが現実です。
RWEの代表的な活用シーン
実務でRWEが使われる場面は、大きく次の3つに整理できます。
- 承認申請の補完エビデンス:希少疾患や小児、難治性がんなど、RCTの規模を確保しづらい領域で、RWDを用いた外部対照群を補強的に提示する
- 市販後の安全性・有効性監視:再審査・再評価、PASS(承認後安全性試験)でのシグナル検出。ICH M14ドラフトで国際的な手順が整理されつつある
- 適応拡大・効能追加:新たな患者集団や使用条件における有効性・安全性を、RCTを再度実施せずRWEで裏付ける
特に注目度が高いのが外部対照群(External Control Arm; ECA)としての活用です。これは、対照群をプラセボや実薬群として新たに組み込むのではなく、既存のRWDから患者背景を揃えて「合成された対照群」を作る発想です。次のセクションで構築フローを詳しく見ていきます。
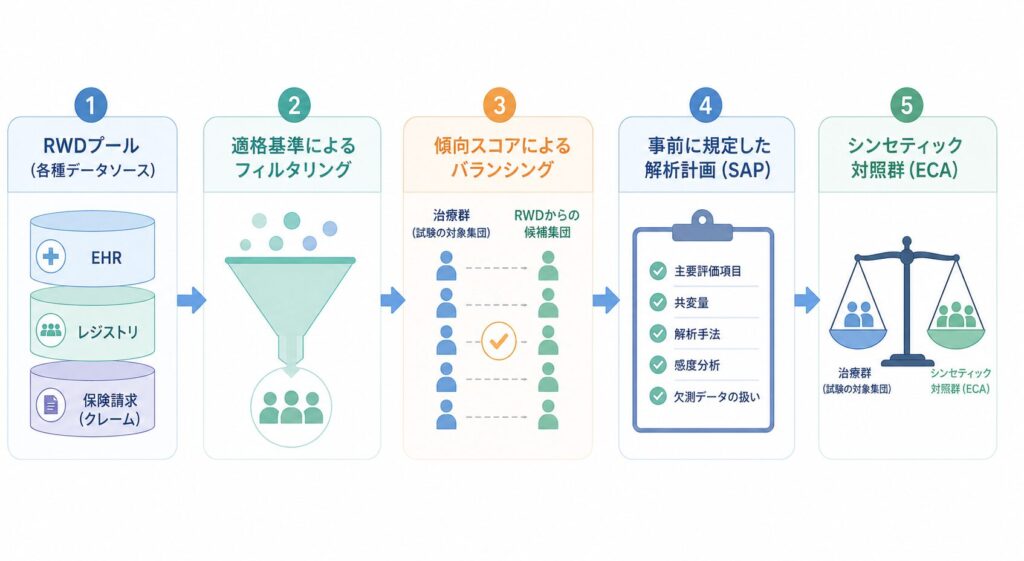
外部対照群(ECA)の構築フロー
外部対照群を構築するときは、勘や経験ではなく事前に文書化した手順で進めることが規制対応の前提になります。最低限のステップは次の5段階です。
- データソースの選定:レジストリ/電子カルテ/レセプトのうち、治療群の集団に最も近い母集団を含むデータソースを選ぶ。データの代表性・追跡可能期間・エンドポイント取得可能性をIMDRFの6視点で評価する
- 適格基準の翻訳:試験プロトコルの組入れ・除外基準を、RWD側で再現できる変数(ICDコード/薬剤コード/検査値)に置き換える。ここで再現できない基準があれば、感度分析で影響を確認する
- 共変量の特定とバランシング:治療効果を歪める交絡因子(年齢/性別/重症度/併用薬/合併症など)を事前に列挙し、傾向スコアやMAIC(Matching-Adjusted Indirect Comparison)で群間バランスを取る
- 解析モデルの事前指定:効果指標(HR・リスク比・差)と解析モデル(Cox回帰/IPTW重み付け/Doubly Robust推定)を解析計画書(SAP)に固定する。modelの後付け選択は規制側に最も嫌われる
- 感度分析と頑健性評価:未測定交絡を仮定したE-value、スコアキャリパーの変更、解析対象集団の入れ替えなど、複数の仮定下で結論が安定するかを確認する
特に重要なのが 3番目のバランシング です。傾向スコアの取り扱いについては、過去記事傾向スコア分析を用いた交絡調整 ― 製薬業界における実務応用とRによる実装で実装まで解説しているので、本記事の補完として参照してください。マッチングとIPTWの違い、共変量バランス(SMD<0.1の目安)、トリミングの考え方など、ECA構築の8割はここで決まります。
ECA・RWE設計を体系的に学ぶなら、本記事末尾で紹介する3冊の参考書籍が最短ルートです。特に薬剤疫学の枠組みでRWDを扱う作法は、独学だと事故りやすいポイントです。本記事下部の📚参考書籍セクションもあわせてご活用ください。
数式で書くと、IPTWは個人 \(i\) の傾向スコア \(e_i = \mathrm{Pr}(T_i=1 \mid X_i)\) を用いて
\[ w_i = \frac{T_i}{e_i} + \frac{1 – T_i}{1 – e_i} \]
という重みで治療群と対照群を再構成します。ここで \(T_i\) は治療割付(治療=1, 対照=0)、\(X_i\) は共変量ベクトルです。MAICはこの考え方を「個別データのある自社試験」と「集計値しか公表されていない競合試験」に拡張したもので、自社の患者重みを動かして競合試験のベースライン平均に揃えます。
統計的バイアスとよくある落とし穴
RWEは「観察データ」を扱うため、RCTでは考えなくてよかった種類のバイアスが顔を出します。代表的なものを押さえておきます。
- 未測定交絡(Unmeasured Confounding):レセプトには検査値や重症度が入っていない、電子カルテにはアウトカム外来時の自覚症状が抜けている、など。E-valueや陰性対照アウトカムで頑健性を評価する
- イムモータルタイムバイアス:治療群が「治療を始めた瞬間から観察」、対照群が「診断時点から観察」のように観察開始がずれることで、治療群が見かけ上長生きに見える現象。ランドマーク解析やtime-varying共変量で対応
- 選択バイアス/インデックス日のずれ:適格基準で組入れ可能となった日(インデックス日)の定義が群間で違うと、結果が歪む
- エンドポイント定義の異質性:RWDで「死亡」「再発」をどう同定するかは、コードベースで定義することが多く、感度分析で複数の定義を試すべき
このうち、対照群選択の妥当性に直結する論点は、ICHガイドライン【徹底解説】ICH E10「臨床試験における対照群の選択」でも整理されているので、外部対照群を扱うときの規制側の論点として併読しておくと役立ちます。また、層別による交絡調整の考え方は層別解析により因果効果を推定する―― 製薬業界で働く人のための実践的ガイドを参照してください。
RWE活用のこれからと実務でのポイント
RWEは適応的デザインやベイズアプローチとも相性が良く、たとえば外部対照群の情報を事前分布としてベイズ流のborrowing(情報借用)で取り込むハイブリッド設計は、希少疾患領域で実装が進みつつあります。アダプティブデザインの最新動向はICH E20(臨床試験のためのアダプティブデザイン)でも整理しています。
- RWEは「データ品質×解析設計×事前協議」の三位一体。どれか一つでも欠けると承認申請には使えない
- 外部対照群はSAPと感度分析計画を解析前に固定。事後選択は規制側に必ず指摘される
- 傾向スコア・MAIC・E-value・ランドマーク解析は標準ツールキットとして揃えておく
- ICH M14ドラフトとFDA医療機器2025年最終ガイダンスは、自社のSOPに早めに反映させる
📚 この記事をより深く理解するための参考書籍
リアルワールドデータと外部対照群の運用を体系的に学びたい方に、特におすすめできる3冊です。



関連記事・次のステップ
- 【徹底解説】ICH E10「臨床試験における対照群の選択」 ― 外部対照群を扱うときの規制側の論点を体系化
- 傾向スコア分析を用いた交絡調整 ― 製薬業界における実務応用とRによる実装 ― ECA構築の中核手法のRコード付き解説
- 層別解析により因果効果を推定する ― 製薬業界で働く人のための実践的ガイド ― 層別の発想で交絡を理解する基礎
- ICH E20(臨床試験のためのアダプティブデザイン)とは ― RWE×アダプティブで広がる試験デザイン
まとめ
本記事では、リアルワールドエビデンス(RWE)の基本概念、FDA・PMDA・EMAの最新動向、外部対照群(ECA)の構築フロー、そして実務で必ずぶつかるバイアスまでを整理しました。RWEはRCTを置き換えるものではなく、RCTで届かない領域を補完してエビデンスを立体化するためのツールであり、データ品質・解析設計・規制との事前協議のすべてをそろえることが必須要件になります。
特に、外部対照群は希少疾患・がん領域での承認申請を後押しする強力な選択肢ですが、傾向スコア・MAIC・E-valueなどの統計手法を抑えていないと、規制対応のステージで頓挫しかねません。本記事で紹介した3冊の参考書籍と関連記事を活用しながら、自社のSOPに2024〜2025年の規制動向を早めに反映していただければと思います。
次回以降は、外部対照群の具体的な実装例(傾向スコアマッチング・IPTW)をRコード付きで掘り下げる記事や、マスタープロトコル試験との接続を扱う記事を予定しています。