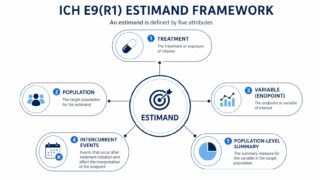
マスタープロトコル試験とは ― バスケット・アンブレラ・プラットフォームの違いと規制動向 ―
・マスタープロトコル試験の基本概念と、なぜ近年急速に注目されているのか
・バスケット試験・アンブレラ試験・プラットフォーム試験の違いと使い分け
・ベイズ流の情報借用や多重性調整など、統計的に押さえるべきポイント
・FDA・厚労省・PMDAのガイダンス動向と、実装上の留意点
記事の目次
Toggleはじめに
近年、希少疾患・がん領域の医薬品開発では、対象患者が少なく従来型の無作為化比較試験(RCT)を組むことが極めて困難な場面が増えています。そこで世界の規制当局・製薬企業が注目しているのが マスタープロトコル試験(master protocol trial) です。1つの「親プロトコル」のもとで複数のサブスタディを同時並行・継続的に走らせることで、開発期間とサンプルサイズを大きく圧縮できる新しい試験設計の枠組みです。
本記事では、製薬業界の生物統計担当者・申請業務担当者・臨床開発企画担当者を念頭に、マスタープロトコル試験の3つの代表的デザインである バスケット試験・アンブレラ試験・プラットフォーム試験 を整理し、統計的特徴と規制当局の動向、さらに実装上の留意点までを体系的に解説します。
1. マスタープロトコル試験とは
マスタープロトコル試験とは、1つの試験計画書(マスタープロトコル)に複数のサブスタディを組み込み、共通のインフラ・対照群・データ管理基盤を共有しながら複数の薬剤や疾患を同時に評価する臨床試験の枠組みです。FDAの2023年ドラフトガイダンス「Master Protocols for Drug and Biological Product Development」では、これまで個別に走らせていた試験を1つの傘の下に集約することで、被験者の負担軽減・対照群の効率的活用・開発スピードの加速が期待できると整理されています。
厚生労働省も2024年6月20日付の事務連絡「医薬品開発等におけるマスタープロトコル試験の活用に関する留意事項」を発出し、日本でも開発計画の選択肢として正式に位置づけられました。1つの薬剤と1つの疾患の組み合わせごとにプロトコル・治験届・施設立ち上げを繰り返す従来の枠組みに比べると、マスタープロトコルは 「試験」ではなく「試験を生み出す仕組み」 と捉えるのが適切です。
マスタープロトコル試験は「アダプティブデザインの一種」と誤解されがちですが、両者は別概念です。アダプティブデザインは「途中で計画を変更する仕組み」、マスタープロトコルは「複数のサブスタディを1枚の傘で束ねる枠組み」を指します。両者は組み合わせて使われることが多いものの、定義は分けて理解する必要があります。
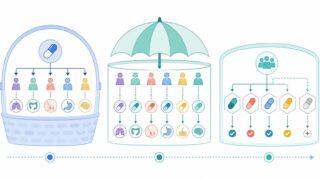
2. 3つのデザイン:バスケット・アンブレラ・プラットフォーム
マスタープロトコルには、評価対象が「薬剤」と「疾患」のどちらに広がるかで3つの代表的なバリエーションがあります。厚労省事務連絡の定義をもとに、以下のように整理できます。
| デザイン | 薬剤 | 疾患 | 主な目的 |
|---|---|---|---|
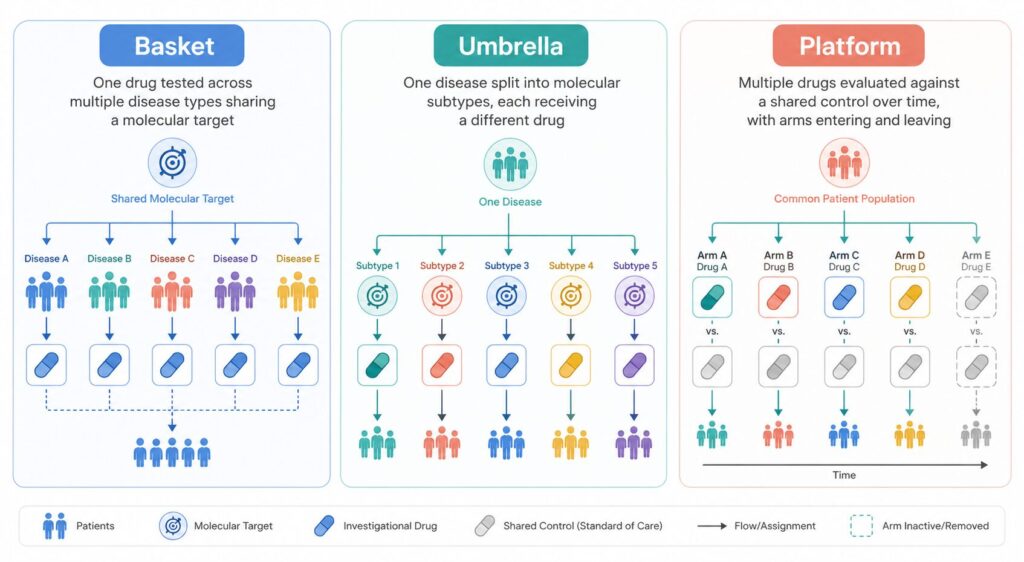
| バスケット試験 | 単一 | 複数 | 分子標的が共通する複数疾患でのPOC評価(探索的) |
| アンブレラ試験 | 複数 | 単一 | 同一疾患のサブグループに最適な薬剤を割り付け |
| プラットフォーム試験 | 複数(追加・除外あり) | 単一または複数 | 継続的に薬剤を入れ替えながら長期評価 |
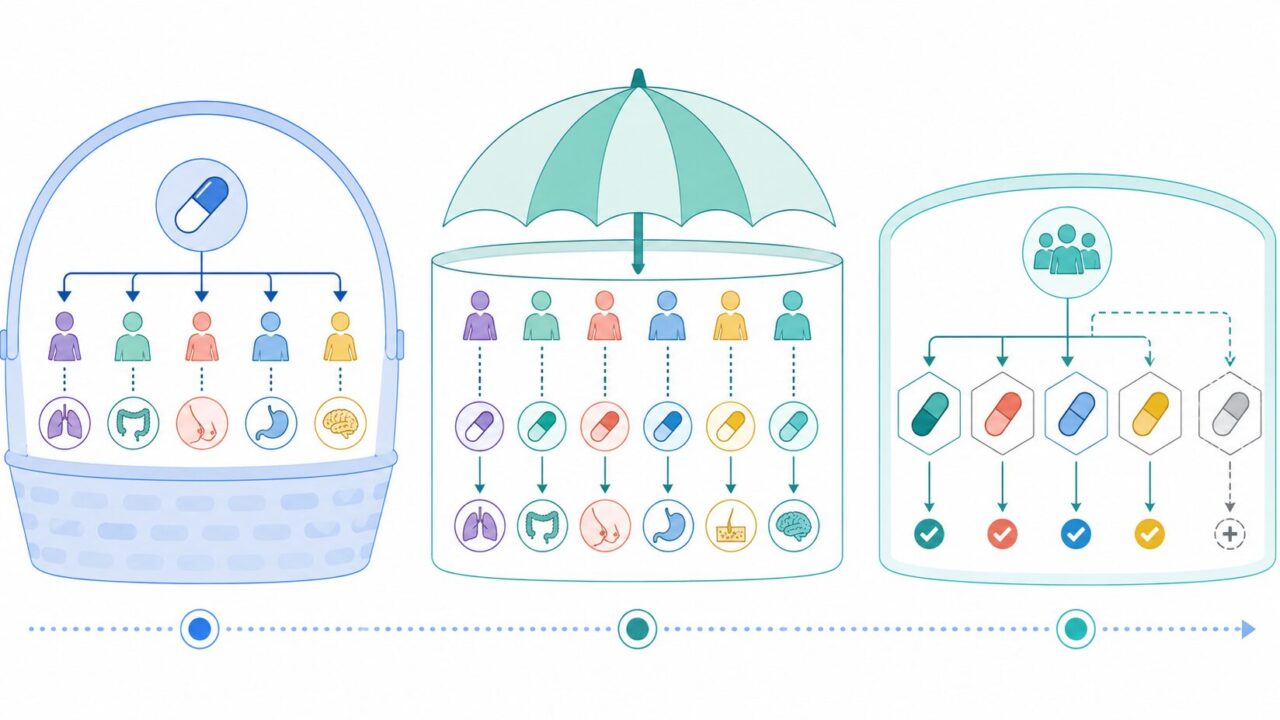
2.1 バスケット試験
バスケット試験は、ある共通の生物学的標的(ドライバー遺伝子変異など)を持つ複数の疾患群に対して、1つの薬剤を投与する設計です。例えば「BRAF V600E変異を持つメラノーマ・甲状腺がん・大腸がん」を一つの試験で評価し、疾患横断的に有効性のシグナルを拾います。希少疾患や腫瘍領域での POC(proof-of-concept)試験 として用いられることが多く、迅速にバイオマーカー駆動型の開発判断ができる点が大きな利点です。
2.2 アンブレラ試験
アンブレラ試験は逆に、1つの疾患を分子サブグループに分け、それぞれに最適な薬剤を当てる設計です。非小細胞肺がんのドライバー変異別の治療最適化や、乳がんのHER2/HR別の試験などが代表例です。患者ごとに最も効きそうな薬剤を割り付けるため、被験者の倫理的負担が小さく、リクルート効率も高くなります。
2.3 プラットフォーム試験
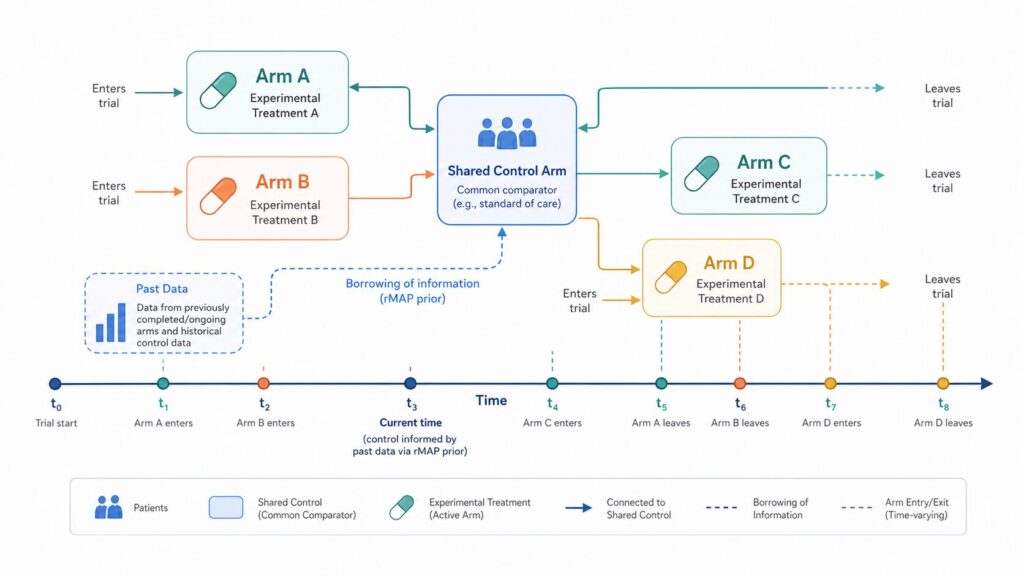
プラットフォーム試験は、あらかじめ終了時点を決めず、薬剤を試験中に追加・脱落させながら継続的に評価する設計です。COVID-19対応で世界的に注目された英国のRECOVERY試験や、乳がん術前化学療法のI-SPY 2が有名な実例です。共通の対照群を長期にわたり共有できるため、薬剤あたりの必要被験者数を大幅に減らせる点が最大の魅力です。
3. 統計的に押さえるべき特徴
マスタープロトコル試験は単なる「試験のまとめ方」ではなく、統計的に新しい論点をいくつも生みます。以下では実装上特に重要な3点を整理します。
3.1 共通対照群と情報借用(borrowing)
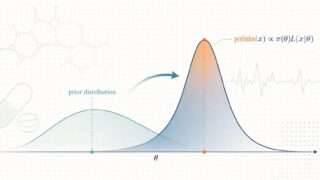
プラットフォーム試験では、複数の試験アームが時間的にずれながら共通対照群と比較されます。同時期の対照群(concurrent control)と過去の対照群(non-concurrent control)をどう統計モデルに組み込むかが大きな論点で、ベイズ流の階層モデルや、頻度論側でのロバストな調整法が研究されています。とくに 事前情報を借用する Robust Meta-Analytic Predictive (rMAP) 事前分布 は、希少疾患領域で実装例が増えています。
事前分布を \(\pi_0(\theta)\)、観測データの尤度を \(L(\theta\mid D)\) とすると、事後分布は
\[ \pi(\theta\mid D) \propto L(\theta\mid D)\cdot \pi_0(\theta) \]
と書けます。ここで \(\theta\) は対照群の真の効果(奏効率や平均値)で、過去データから構築した \(\pi_0(\theta)\) をどの程度信頼するかが、現在試験のサンプルサイズ削減幅と直結します。
3.2 多重性の制御
複数のサブスタディを並列に走らせると、第一種の過誤(false positive)の累積が問題になります。サブグループごとに別個の試験として扱うのか、ファミリーワイズ誤り率(FWER)を全体で制御するのか、あるいは偽陽性の期待数(FDR)に切り替えるのか――この設計判断が試験全体の妥当性を決めます。FDAは2023年ガイダンスで「多重性の制御方針を事前に明文化すること」を強く推奨しています。
3.3 適応的要素との組み合わせ
プラットフォーム試験はほぼ例外なく、群逐次デザインや反応適応的無作為化、無益性中止などのアダプティブな要素と組み合わせて運用されます。途中解析の都度、サンプルサイズや割り付け比を更新する仕組みは、試験全体の運用負荷を増やす一方で、開発資源の効率的配分を可能にします。アダプティブデザインの基本については、後半で紹介する書籍が詳しく扱っています。
マスタープロトコル試験のメリットは「サンプルサイズ削減」「対照群共有」「開発加速」の3点に集約されます。一方で、デメリットとしては「統計的設計の複雑化」「試験運営コストの増大」「途中追加薬剤の比較可能性確保の難しさ」が挙げられ、設計段階でPMDAやFDAとの事前相談が事実上必須となります。
📚 より深く学ぶなら
マスタープロトコル試験の統計設計をきちんと体系立てて学びたい方には、後半で紹介する朝倉書店『臨床試験のためのアダプティブデザイン』『臨床試験の事典』が特におすすめです。臨床試験デザイン全般の基礎を固めたうえで、最新の論文(FDAガイダンス・厚労省事務連絡など)と並行して読むのが実務上の最短ルートです。
4. 規制当局の動向
4.1 FDA:2023年ドラフトガイダンスで枠組みを統合
FDAは2023年に「Master Protocols for Drug and Biological Product Development」のドラフトガイダンスを発出し、それまでに個別領域で出していたCOVID-19(2019)、腫瘍領域(2022)、細胞・遺伝子治療(2022)の各ガイダンスを統合・拡張しました。汎領域での適用を視野に入れた整理がされており、これを参照することでスポンサー側の議論が一段とスムーズになります。
4.2 厚労省・PMDA:2024年事務連絡で日本でも本格運用へ
日本では2024年6月、厚労省医薬局医薬品審査管理課から「医薬品開発等におけるマスタープロトコル試験の活用に関する留意事項」が事務連絡として発出されました。3デザインの定義・想定される目的・統計的留意事項・PMDA事前相談の活用がコンパクトに整理されており、国内臨床試験ガイドライン体系の基準書として機能しています。
4.3 ICH E20との関係
2026年にFinalizeされたICH E20「Adaptive Designs for Clinical Trials」は、アダプティブデザイン全般を扱うガイドラインで、プラットフォーム試験における追加割付や中間解析もスコープに含まれます。マスタープロトコル試験を採用する際は、ICH E20の枠組みに沿って計画書を整備するのが標準的な進め方になります。
5. 実装上の留意点
マスタープロトコル試験を実務で立ち上げる際に、生物統計担当者として押さえておきたい論点を最後にまとめます。
- マスタープロトコルとサブスタディの責任分界:マスタープロトコル本体と各サブスタディの治験責任医師・スポンサー責任を明確にする。
- 共通対照群の取り扱い:時間的バイアスを抑えるため concurrent control を可能な限り維持し、必要に応じて時期を共変量として調整する。
- 多重性の事前計画:FWER/FDRどちらで制御するかを必ず事前に決め、各サブスタディの仮説体系を明文化する。
- サンプルサイズ・無益性中止基準の更新ルール:途中解析の都度ルールを決めておき、運営委員会・DMC(データモニタリング委員会)の責務を分離する。
- 規制当局事前相談:日本ではPMDAの治験相談、米国ではFDAのType B/C ミーティングを早期に実施し、デザインの妥当性について合意を得ておく。
マスタープロトコル試験は、希少疾患・腫瘍・パンデミック対応などサンプルサイズ確保が困難な領域で特に威力を発揮します。生物統計担当者は「3デザインの違い」「共通対照群の使い方」「多重性と適応性の事前計画」を押さえたうえで、PMDA/FDAとの事前相談を主導することが期待されます。
関連記事・次のステップ
- ベイズ統計入門:頻度論との違いとベイズの定理 — マスタープロトコル試験で使われる情報借用やrMAP事前分布を理解する前提として最初に読みたい記事です。
- ベイズ統計における事前分布・事後分布・尤度の関係と共役事前分布 — 共通対照群の情報借用に直結する事前分布の設計を、数式と直感で解説しています。
- 臨床試験における多重比較法 ― グラフィカルアプローチの魅力と実践 — 複数サブスタディの多重性制御を考える際の基礎となる手法を解説しています。
まとめと次回予告
本記事では、マスタープロトコル試験の3つの代表的デザイン(バスケット・アンブレラ・プラットフォーム)の違い、ベイズ流の情報借用や多重性などの統計的特徴、FDA・厚労省・PMDAのガイダンス動向、そして実装上の留意点を整理しました。希少疾患・腫瘍・新興感染症の領域でますます重要性を増す枠組みであり、生物統計担当者にとっては必須リテラシーになりつつあります。
次回は、本記事で触れた 「共通対照群と情報借用」 の中核技術である RECOVERY試験・I-SPY 2試験のケーススタディ を取り上げ、実際の試験運営でどのように適応的要素が組み込まれたかを具体的に解説します。マスタープロトコル試験の理解をさらに深めていただければと思います。