ITT・FAS・PP・mITT の違いを完全整理 ― ICH E9 が定める臨床試験の解析対象集団 ―
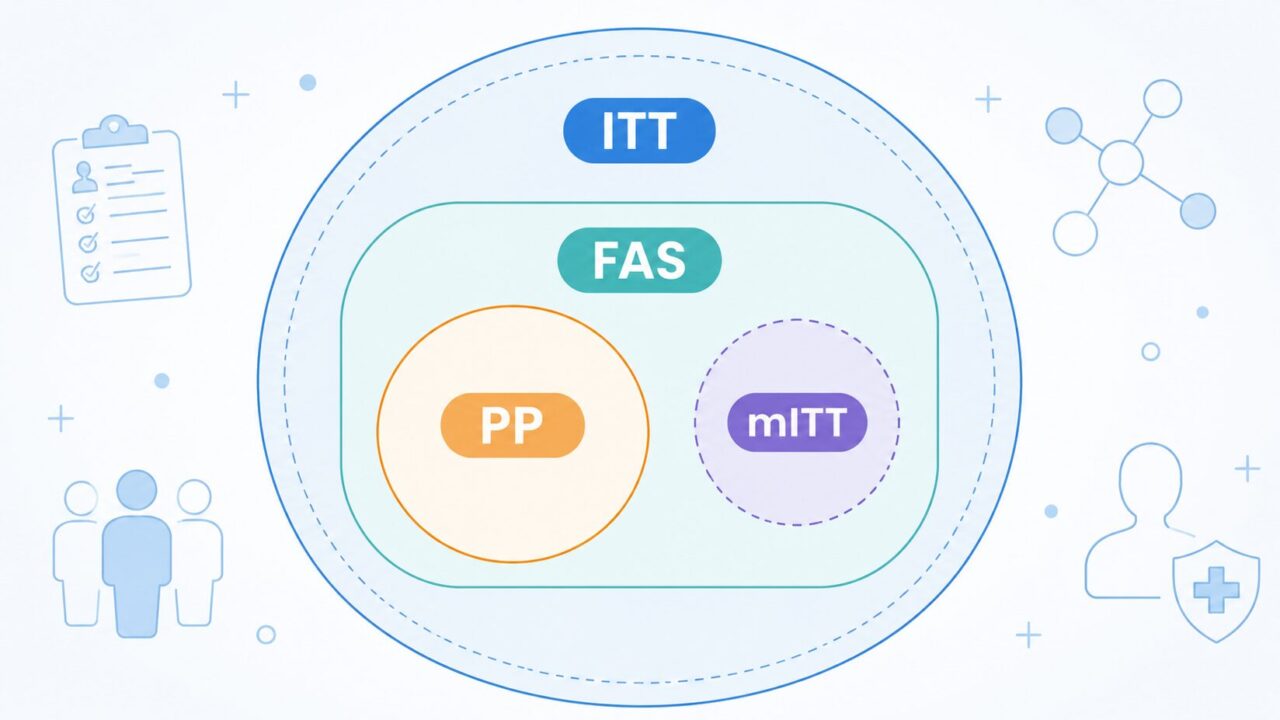
・ITT(Intention-to-Treat)、FAS(Full Analysis Set)、PP(Per Protocol Set)、mITT(modified ITT)の4つの解析対象集団それぞれの定義
・ICH E9『臨床試験のための統計的原則』および ICH E9 (R1) 補遺(Estimand)との関係性
・4集団の使い分け、主要解析と感度分析の組み合わせ方を実務目線で
・PMDA・FDA・EMA など規制当局がどの集団をどう評価するかの視点
・脱落・治療未開始・重大プロトコル違反など、実務で頻出する落とし穴と対処法
記事の目次
Toggleはじめに
ランダム化比較試験(RCT)の有効性評価において、「誰を解析対象に含めるか」という問いは、得られる結論を大きく左右する極めて重要な論点になります。ランダム化によって担保されたはずの群間比較可能性も、解析対象の選び方ひとつで容易に揺らぎ得るのが現実です。こうした問題意識のもと、ITT・FAS・PP・mITT といった解析対象集団の概念は、ICH E9『臨床試験のための統計的原則』(1998年)によって国際的に整理され、今日まで臨床開発の標準言語として定着してきました。本記事は、製薬企業の生物統計担当者・臨床開発担当者、CRO のモニターやデータマネジャー、そして統計検定準1級〜1級の受験者を主な対象としています。近年は ICH E9 (R1) 補遺で導入された Estimand フレームワークの文脈においても、「主要解析の対象集団をどう定義するか」が改めて注目されており、本テーマの実務的重要性は一段と高まっているといえます。
解析対象集団の全体像 ― なぜ複数のセットが必要か
そもそも、なぜ臨床試験の解析では複数の集団を定義する必要があるのでしょうか。その答えは、臨床試験が答えるべき問いが一つではないという点に集約されます。
第一に、ランダム化比較試験の最大の強みは、ランダム化によって群間の比較可能性を担保できる点にあります。この強みを最大限に活かすには、ランダム化された被験者を全員、割り付けられた群に属するものとして解析する原則 ― すなわち Intention-to-Treat(ITT、治療意図に基づく解析)の原理が不可欠になります。ITT は「ランダム化後に脱落した被験者や治療を中断した被験者も、初期割り付け群のまま解析する」というシンプルかつ強力な原則であり、選択バイアスを最小化する観点から規制当局も第一に重視する考え方です。
第二に、臨床現場の医師や患者にとっては、「プロトコル通りに治療を完遂した場合の純粋な治療効果」を知りたいというニーズも当然存在します。これは Per Protocol 的な視点と呼ばれ、ITT とは異なる問いに答えるものです。さらに、安全性評価では実際に治験薬を1回でも投与された集団(Safety Set)で評価するのが標準であり、有効性と安全性で集団が異なるのが通例になります。
第三に、規制当局は単一の解析結果だけでは納得しません。主要解析の結論が解析対象集団の選択に対して頑健であることが求められ、「主要解析+感度分析」の組み合わせで結論の安定性を示すのが現代の標準的アプローチになっています。
こうした要請に応える形で、ICH E9(1998年策定)は、ITT の原則を実務に落とし込むための運用概念として Full Analysis Set(FAS、最大の解析対象集団)と Per Protocol Set(PPS、治験実施計画書遵守集団)を整理しました。ここで重要なのは、ITT はあくまで「原則」であり、FAS と PPS はその運用上の実装として位置づけられているという階層関係です。一方の modified ITT(mITT、修正 ITT)は ICH E9 に明示的な定義が存在せず、試験ごとに「最低1回投与を受けた被験者に限定する」「ベースライン後の評価が1回以上ある被験者に限定する」など、個別に定義されるのが実態になります。この曖昧さこそが、mITT が後発的に議論を呼ぶ一因にもなっています。
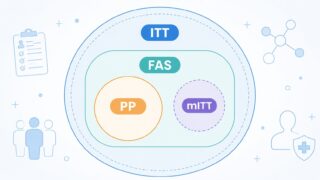
集団選択の影響は決して机上の話ではありません。例えば、ランダム化後に治療を一度も受けなかった被験者を解析から除外するか否か、重大なプロトコル違反者を主要解析に含めるか否かといった判断は、有効性の推定値そのものを変動させ得る要素になります。下図のような階層関係を意識すると、各集団の位置づけがより直感的に理解できます。
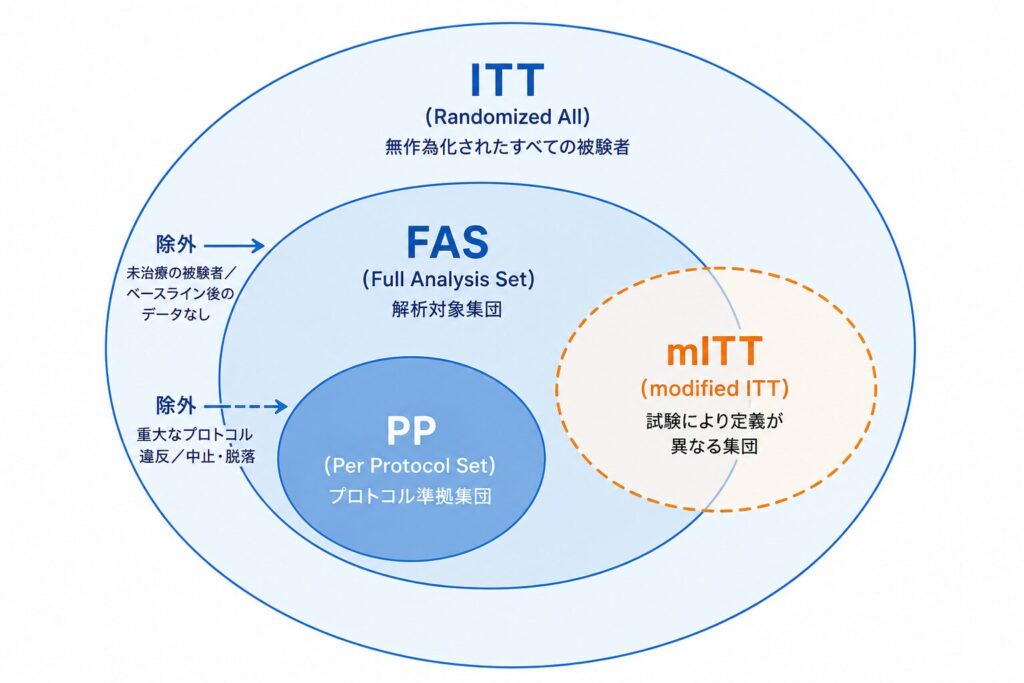
次章以降では、それぞれの集団の定義と実務上の運用ルールを、ICH E9 の原文に即して一つずつ丁寧に確認していくことにいたします。
ITT・FAS・PP・mITT の定義整理
本章では、臨床試験の解析対象集団として用いられる4つの代表的な集団、すなわち ITT・FAS・PP・mITT のそれぞれについて、定義・起源・実務上の運用を整理します。これらは似て非なる概念であり、混同すると試験結果の解釈を誤る原因になります。ICH E9 ガイドラインを軸に、規制実務での扱いまで踏み込んで解説します。
ITT(Intention-to-Treat、治療意図に基づく解析)
定義:ITT とは、ランダム化された全被験者を、実際に受けた治療内容ではなく当初の割付通りの群で解析する原則を指します。たとえ被験者が割付と異なる治療を受けたり、途中で脱落したりした場合でも、ランダム化された群のまま解析に含めるのが ITT の核心です。
この考え方の起源は、1961 年に英国の統計学者 Sir Austin Bradford Hill が著書『Principles of Medical Statistics』のなかで提唱したものとされ、その後 1990 年代にかけて国際的に標準化されていきました。現在では ICH E9(1998 年)が ITT の原則を明示的に支持しており、世界の医薬品開発の共通言語となっています。
ITT の理念は明快で、ランダム化によって担保された群間の比較可能性を維持し、選択バイアスを排除することにあります。割付後にどのような理由であれ被験者を除外すると、その除外が結果と相関する可能性が生じ、ランダム化の恩恵を失います。
ただし「純粋な ITT」は実務では極めて困難です。全被験者から完全なアウトカムデータを収集する必要があり、脱落や測定欠測があると成立しません。そこで ICH E9 は、ITT の理念を実務的に近似する運用概念として、次に述べる FAS を用いることを推奨しています。
FAS(Full Analysis Set、最大の解析対象集団)
定義:FAS とは、ITT の理念を実務的に近似するために設定される集団であり、ランダム化された全被験者から割付と無関係な理由でのみ除外を行ったうえで構成される、可能な限り ITT に近い集団です。
ICH E9(Statistical Principles for Clinical Trials)では、FAS から除外することが許容される理由を限定的に列挙しています。具体的には次の3つが代表的です。
- 適格基準を満たさないことがランダム化後に判明したケース(いわゆる誤組み入れ)
- 治験薬を一度も投与されていないケース
- ランダム化後のデータが一切得られていないケース
これらの除外が許容されるためには、厳格な条件があります。すなわち、除外基準がランダム化前にプロトコルに明記されていること、そして除外の有無がアウトカムと独立であることです。事後的な恣意的除外は、たとえ妥当に見えてもバイアスの温床となり、規制当局から否定的に評価されます。
規制実務での扱いとしては、多くの優越性試験において FAS が主要解析集団として採用されます。これは、ITT 原則を最も忠実に近似しながら現実のデータ運用と整合させるバランスが取れているためです。
一方で、非劣性試験においては FAS の使用がしばしば結果を中立側(差がない方向)に引き寄せる性質を持つため、FAS のみでの判定では誤った非劣性結論を導くリスクが指摘されています。このため非劣性試験では PP と FAS の両方で一貫した結論が得られるかを確認するのが標準的な運用です。この点は後の章で詳しく解説します。
PP(Per Protocol Set、プロトコル順守集団)
定義:PP とは、FAS(または ITT)からさらにプロトコルからの主要な逸脱者を除外し、計画通りに試験を完遂した被験者のみで構成される集団です。
主な除外対象は以下のとおりです。
- プロトコル違反(規定外の用量、投与期間、禁止併用薬の使用 など)
- コンプライアンスの著しい低下(服薬率が事前定義の閾値を下回る など)
- 主要評価項目の測定欠落や測定時期の逸脱
- 事後的に判明した主要な選択基準違反
PP の性質は、「治療を計画通りに完遂した被験者集団」での効果を評価する点にあり、「効力(efficacy)」に近い解釈が可能になります。理想条件下での薬剤の真の効果に迫る集団とも言えます。しかし一方で、除外が事後的に行われるため、除外された被験者と残った被験者の間にアウトカム関連の差が生じやすく、選択バイアスのリスクが大きい点に留意が必要です。
非劣性試験では、FAS と PP の両方を主要解析の対象とし、両解析で同一の結論が得られることを確認するのが標準的なアプローチです。ICH E9 および FDA・PMDA をはじめとする規制当局も、この二重確認の枠組みを支持しています。
mITT(modified ITT、修正ITT)
定義:mITT とは、ITT から特定の事前定義された理由で被験者を除外して構成される集団です。ICH E9 には明示的な定義は存在せず、試験ごとにプロトコルで具体的に定義する必要があります。
典型的な除外パターンとしては、次のようなものが挙げられます。
- 治験薬を一度も投与されていない被験者
- ランダム化後の有効性データが一切ない被験者
- 適格基準違反が事後的に判明した被験者
これらの除外パターンを見れば分かるとおり、mITT は FAS と概念的に重なる部分が非常に多く、文献によっては FAS と mITT を実質的に同義として扱う場合もあります。実務上、両者の境界はしばしば曖昧です。
mITT の定義は試験ごとに大きく異なります。同じ「mITT」という名前でも、ある試験では「治験薬を1回でも投与された被験者」を指し、別の試験では「ベースライン後に有効性評価が1回以上行われた被験者」を指すなど、内容が一致しないことが珍しくありません。この定義の不透明さがバイアスの温床となり、解析対象を恣意的に絞ることで結果を有利に見せる「mITT による結果操作」が問題視されてきました。FDA・PMDA をはじめとする規制当局は、mITT を用いる場合にはその定義をプロトコルに厳格に明記し、ランダム化前に固定することを強く求めています。論文や治験総括報告書を読む際は、mITT の定義を必ず確認する習慣をつけましょう。
4集団の比較と決定フロー
ここまで ITT・FAS・PP・mITT の4集団について、それぞれの定義と背景を個別に確認してきました。実務でこれらを使い分ける際には、4集団を横並びで比較し、どの場面でどの集団が主役になるのかを俯瞰しておくことが欠かせません。以下では、まず比較表で定義と用途を整理し、続いて主要解析集団を選ぶ際の決定フローを示します。
| 集団名 | 定義の要点 | 除外される典型例 | 主な用途 | バイアスの方向 |
|---|---|---|---|---|
| ITT | 無作為化された全被験者を割付通りに解析 | 原則として誰も除外しない | 優越性試験の主要解析(理念上の基準) | 群間差を小さくする方向(保守的) |
| FAS | ITT に最も近い実務的集団。最小限の除外を許容 | 登録後に治験薬を一度も投与されなかった例、ベースライン欠測 等 | 優越性試験の主要解析/非劣性試験の主要解析の一方 | ITT 同様、群間差を小さくする方向 |
| PP | プロトコルを遵守し完遂した症例のみで解析 | 服薬コンプライアンス不良、重大な逸脱、中止例、欠測例 | 非劣性試験の主要解析(FAS と併用)/感度分析 | 治療効果を過大評価する方向(選択バイアス) |
| mITT | 事前定義に基づき限定的に除外した修正版 ITT | 適格基準違反、治験薬未投与、ベースライン評価未実施 等(プロトコル事前規定) | 主要解析(FAS の代替)/感度分析 | 除外基準の設定次第で変動(事前明記が必須) |
表を縦に眺めると、解析対象者数は ITT ≧ FAS ≒ mITT > PP の順に小さくなる傾向があります。バイアスの向きで言えば、ITT と FAS は「群間差を埋める方向」に働きやすく結論として保守的、PP は完遂者に偏ることで「治療側に有利」になりやすい点が対照的です。mITT は除外基準の設計が結果に直結するため、プロトコル事前規定が運用上の生命線になります。
続いて、実務で「どの集団を主要解析にするか」を判断するためのフローを次に示します。試験タイプ・主要評価項目の性質・脱落の見込み量という3軸から、最適な解析集団を選ぶ流れを視覚化したものです。
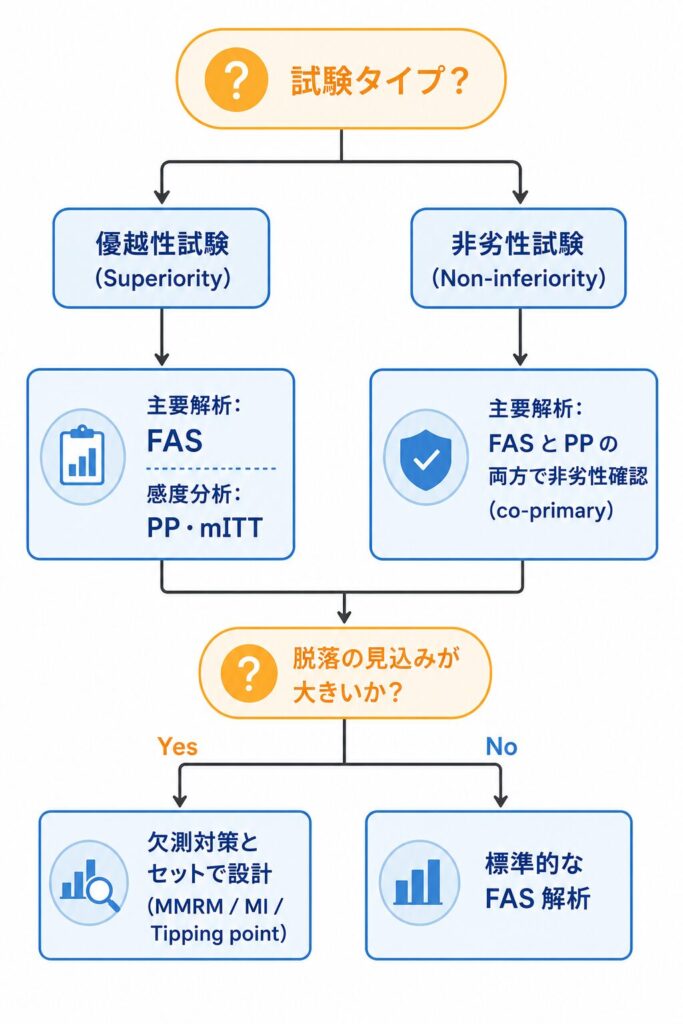
判断軸を実務目線で整理すると、優越性試験では FAS を主要解析に据え、PP を感度分析として配置するのが標準ラインです。一方、非劣性試験では FAS と PP の両方を主要解析に位置づけ、両者で非劣性が確認されることを求められます。さらに、評価項目がイベント発生か連続値かによっても扱いが変わり、脱落が大きく見込まれる試験ではあらかじめ欠測対策とセットで設計しておくことが重要です。
主要解析と感度分析での使い分け(実務ポイント)
優越性試験での標準的な運用は比較的シンプルです。主要解析には ITT に最も近い集団である FAS を用い、無作為化の利点を最大限に活かして群間比較を行います。これに対し、感度分析として PP や mITT、さらにはプロトコル完遂者のみを対象とする完了者解析を併用し、「集団の取り方を変えても結論が揺らがないか」を多面的に確認します。FAS で統計的有意差が得られ、かつ PP でも同じ方向の効果が確認されれば、結論の頑健性が支持されます。逆に FAS と PP で結果が食い違う場合は、欠測や非遵守の影響を考察したうえで慎重に解釈する必要があります。
非劣性試験では事情が大きく異なります。FAS は欠測や非遵守を含めて解析する性質上、群間差を「縮める」方向に働きやすく、これは優越性試験では保守的(差を出にくくする)ですが、非劣性試験では 非劣性が成立しやすい方向に偏ってしまう という逆説的な問題を生じます。この性質を放置すると、実態以上に試験薬が同等に見えてしまう恐れがあるため、規制当局(PMDA・FDA・EMA)は FAS と PP の両方で非劣性が成立する ことを要求します。ICH E9 においても、非劣性試験での FAS 単独評価のリスクは明示されており、二集団での一貫性確認が事実上の必須要件です。
欠測データの扱いも集団選択と密接に絡みます。FAS を採用するなら、欠測値の処理戦略をセットで設計する必要があり、近年は MMRM(Mixed Model for Repeated Measures)、多重代入法(MI)、Tipping point 解析 などが標準的に用いられます。一方、PP は完遂者中心の解析になるため欠測の扱いは比較的緩くなりますが、その代償として完遂者という非ランダムな部分集団に基づく 選択バイアス を抱え込みます。
こうした使い分けは ICH E9 の記述だけで完結するものではなく、臨床試験統計の定番専門書を併読することで、実務上の判断軸が磨かれていきます。FAS と PP の解釈の重み付けや欠測戦略の選び方など、規制ガイドラインの行間に潜む論点を学ぶうえで有用ですので、記事末尾の参考書籍もぜひ併せて参照してください。
・mITT の除外基準は必ずプロトコルに事前明記する。事後的な除外は ITT 原則を損なう
・非劣性試験は FAS と PP の両方で非劣性が成立することを確認する(ICH E9 / 規制当局要件)
・FAS を主要解析にするなら欠測戦略をセットで設計する(MMRM、多重代入法、Tipping point 等)
・PP は仮説検証ではなく解釈の補助に位置づけ、選択バイアスを前提に解釈する
・Estimand framework(ICH E9 R1)では「どの解析集団か」より「何を推定したいのか(推定対象)」の議論が中心となっており、集団選択もこの枠組みの中で再整理されつつある
📚 参考書籍
ITT・FAS・PP・mITT を含む解析対象集団の議論を、より深く実務レベルで使いこなせるようになるための定番書を3冊紹介します。いずれも臨床試験統計の現場で広く参照されている書籍です。



まとめ
本記事では、ICH E9 が定める臨床試験の解析対象集団である ITT・FAS・PP・mITT の違いを整理し、それぞれの定義・除外基準・実務での使い分けまでを一気通貫で解説しました。ITT はランダム化の利点を最大限に活かす理念であり、FAS はその実務的実装、PP はプロトコル順守者に絞った集団、mITT は試験ごとの事前定義に基づく修正版 ITT という階層関係を理解することが第一歩になります。
実務的には、優越性試験では FAS を主要解析・PP を感度分析、非劣性試験では FAS と PP の両方を主要解析、という運用が標準であり、ICH E9 および各国規制当局も同様の見解を示しています。さらに、ICH E9 (R1) 補遺で導入された Estimand フレームワークの登場により、「どの集団を解析するか」だけでなく「何を推定したいのか」というより上位の問いを意識した解析計画が求められる時代になりました。日々の解析計画書(SAP)作成や治験プロトコル設計の際には、本記事の整理を出発点として、必ず最新の規制要件と試験デザインを照合していただければと思います。
関連記事・次のステップ
- 【完全理解】ICH E9「臨床試験の統計的原則」と補遺(Estimand)を徹底解説 ― ICH E9 と (R1) 補遺の全体像を体系的に整理した姉妹記事
- 欠測を伴う経時測定データ解析における MMRM と並べ替え法の新しい推定手法 ― FAS を用いる際に必須となる欠測データ解析手法の解説
- 多重代入法(Multiple Imputation)をSASとRで実装する ― FAS 解析の感度分析として頻用される多重代入法の実装ガイド
次回は、ICH E9 (R1) で導入された Estimand フレームワークを、ITT/FAS の議論と接続させながら詳しく整理した記事を予定しています。