FDA 2026年ベイズドラフトガイダンス徹底解読 ─ Borrowing・Operating Characteristics・規制対話の実務ガイド ─
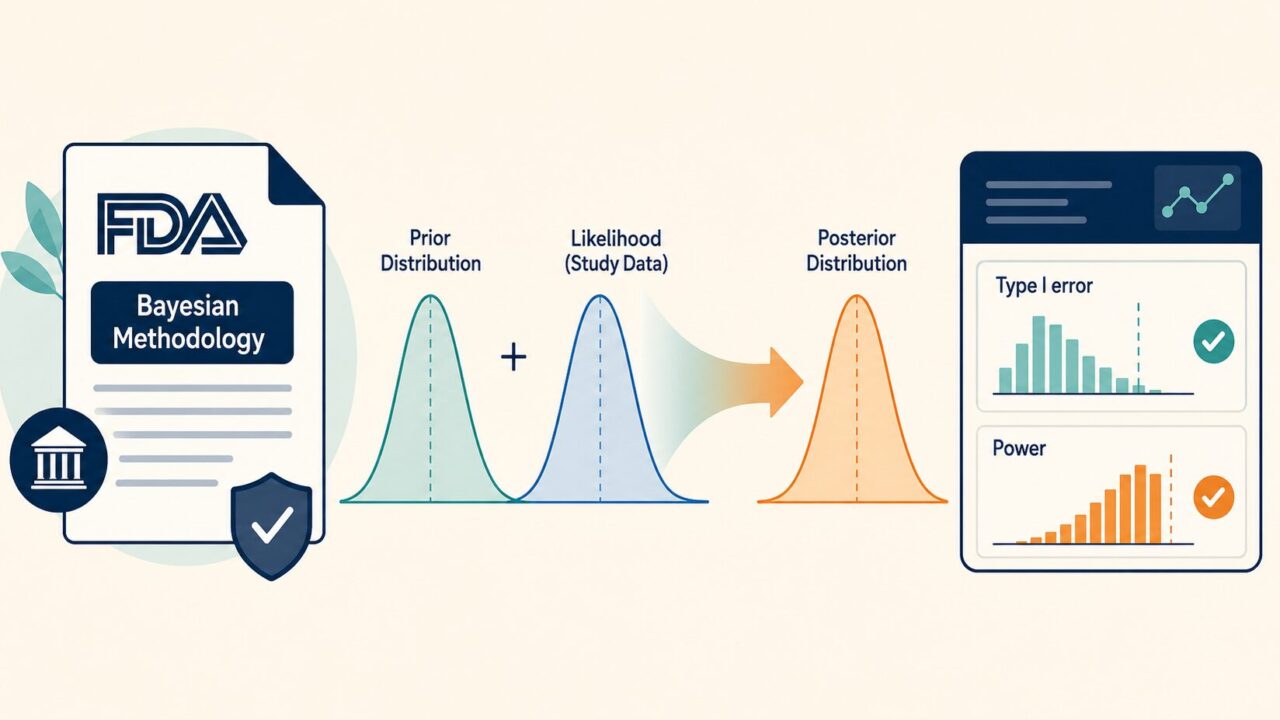
2026年1月、FDAは医薬品・生物製剤を対象としたベイズ統計手法のドラフトガイダンスを公開しました。これは2010年の医療機器向けベイズガイダンス以来、約16年ぶりとなる包括的な規制文書であり、ベイズ流アプローチが「特殊な手法」から「主流の選択肢」へと位置づけを変える歴史的な転換点といえます。本記事では、ガイダンスの全体像、Borrowing(外部情報の借用)とOperating Characteristicsの実務的扱い、そして規制当局との対話に向けた事前準備について、生物統計担当者の視点から徹底的に解読します。Pre-IND・Type B meetingでスポンサーが用意すべき具体的なドキュメント要件まで踏み込んで解説します。
- 2026年1月公開のFDAベイズドラフトガイダンスの正式名称と適用範囲
- ガイダンスが扱う主要トピック(事前分布の正当化・Borrowing・Operating Characteristics・事前キャリブレーション)の全体像
- MAP・Power Prior・Commensurate Prior 3手法の使い分けとRBesTによるRobust MAP実装
- Bayesian power(Assurance)、Type I error、credible interval coverageなど評価指標の規制上の位置づけ
- Pre-IND・Type B meetingに向けてスポンサーが準備すべきBriefing bookの中身と実務上の落とし穴
記事の目次
Toggleはじめに:なぜ2026年がベイズ規制の転換点なのか
ベイズ統計を用いた臨床試験は、これまで医療機器分野や希少疾患領域で限定的に採用されてきました。しかし、FDAが2026年1月に公開したドラフトガイダンス「Use of Bayesian Methodology in Clinical Trials of Drug and Biological Products; Draft Guidance for Industry」(Federal Register Notice 2026-01-12)により、医薬品・生物製剤の領域全体でベイズ流アプローチが正式に位置づけられることになりました。
このガイダンスの最大の意義は、2010年に発出された医療機器向けのベイズガイダンス(”Guidance for the Use of Bayesian Statistics in Medical Device Clinical Trials”)を、医薬品・生物製剤に拡張した点にあります。医療機器領域では事前情報の活用や適応的デザインが比較的早く受容されてきた一方、医薬品開発では頻度論的アプローチが長らく標準でした。今回のドラフトは、その境界線を制度的に取り払うものです。
背景には、希少疾患・小児領域・オンコロジーにおける症例数制約の深刻化、リアルワールドデータ(RWD)や過去試験データを統合する外部対照(External Control)へのニーズの高まり、そしてアダプティブデザインの普及があります。Berry Consultantsをはじめとする業界アドバイザーや解説論文(arxiv 2601.14701ほか)は、本ガイダンスを「borrowingを中心としたガイダンス」と評価しており、predictive probabilityによる無益性中止やレスポンスアダプティブ・ランダム化といったadaptive monitoringの記述は限定的だと指摘されています。つまりFDAは「ベイズ=adaptive design」というイメージから一歩踏み込み、事前分布の正当化と外部情報統合という、より根本的な論点に焦点を当てているのです。
FDA 2026年ドラフトガイダンスの全体像
ドラフトガイダンスは、医薬品・生物製剤の臨床試験全般を対象に、ベイズ流アプローチを採用する際の原則・推奨事項・規制対話の進め方を体系的に示しています。適用範囲はPhase 1からPhase 3、そして承認後試験まで広く、確証的試験(Confirmatory trial)におけるベイズ流主解析の使用も明示的に取り扱われている点が特徴です。
本ガイダンスが扱う主要トピックを整理すると、次の表のようになります。
| トピック | ガイダンスでの扱い | 実務上のポイント |
|---|---|---|
| 事前分布の選択と正当化 | 情報事前分布・非情報事前分布の使い分け、選択根拠の明示 | 専門家エリシテーション、過去試験データの取り扱いを文書化 |
| 外部情報のBorrowing | 過去試験・RWD・ヒストリカル対照の統合手法 | Power prior、Commensurate prior、MAP priorなど動的借用の選択 |
| Operating Characteristics | Bayesian power、Type I error、バイアス、MSE、credible interval coverageの評価を必須化 | 頻度論的指標も併記し、規制当局と共通言語を確保 |
| シミュレーションによる事前キャリブレーション | 事前分布のチューニングと感度分析を事前にシミュレーションで確認 | Prior-data conflictシナリオを含めた網羅的シミュレーション |
| 規制との早期対話 | Pre-IND・Type B meetingでの事前合意形成を強く推奨 | Briefing bookに統計セクションを充実させる |
ここで重要なのは、ガイダンスがベイズ流の利点を強調しつつも、頻度論的なOperating Characteristics、特にType I error rateの制御を依然として要求している点です。Bayesian powerはAssuranceとも呼ばれ、事前分布の下での試験成功確率の期待値として定義される指標ですが、ガイダンスはこれを単独で提示することを認めず、頻度論的な検出力やType I errorとあわせた多面的な評価を求めています。また、credible interval coverage(信用区間が真値を含む頻度論的カバレッジ確率)を評価することで、ベイズ流の区間推定が規制上の解釈と整合しているかを確認するよう促しています。
事前分布の構築:MAP・Power Prior・Commensurate Priorの使い分け
過去試験データを現行試験に取り込む(borrowing:データ借用)ためには、その「重み付け方」を決める事前分布の設計が要となります。FDA 2026年ドラフトガイダンスでは特定の手法を強制してはいませんが、実務で広く用いられているのが MAP prior、Power Prior、Commensurate Prior の3つです。それぞれ「borrowingをどう数学的に表現するか」が異なるため、想定シーンと弱点を理解した上で選択する必要があります。
MAP(Meta-Analytic-Predictive)prior
Neuenschwander et al. (2010, Clinical Trials) が提案した、過去複数試験(historical trials)をベイズ階層モデルで統合する手法です。各試験のパラメータ θₕ が共通の平均 μ と試験間ばらつき τ² から生成されると仮定し、新規試験のパラメータ θ* の予測分布を事前分布として用います。直感としては「メタアナリシスで得られた予測区間を、そのまま次の試験の事前分布として使う」イメージです。
\[ p(\theta_*) = \int p(\theta_* | \mu, \tau) \, p(\mu, \tau | y_{1:H}) \, d\mu \, d\tau \]
τ²(heterogeneity:試験間のばらつき)がデータから推定されるため、過去試験間で結果がばらついている場合には自動的にborrowing量が縮小されるのが長所です。実装は Novartis 製の RBesT::gMAP() で完結します。弱点は、過去試験が3本未満だと τ² の推定が不安定になり、半情報的事前分布(half-normal など)を τ に課す必要がある点です。
Power Prior
Ibrahim & Chen (2000, Statistical Science) による古典的手法で、過去データの尤度を a₀ ∈ [0, 1] で「割引」してから事前分布に組み込みます。a₀ = 1 なら過去データを完全に信用、a₀ = 0 なら完全に無視する、という直感的なパラメトライゼーションです。
\[ \pi(\theta | D_0, a_0) \propto L(\theta | D_0)^{a_0} \, \pi_0(\theta) \]
a₀ を 固定値として事前に指定する方式と、a₀ 自体にBeta事前分布を置く Normalized Power Prior(NPP)方式があります。固定a₀方式は計算が軽く規制当局への説明も容易ですが、heterogeneityへの自動対応がありません。NPPは現データと過去データの整合性に応じてa₀が後方分布的に調整されるため頑健性は高まりますが、正規化定数の計算負荷と感度分析の複雑さが課題です。実装は NPP や rstanarm(一部機能)が利用可能です。
Commensurate Prior
Hobbs et al. (2011, Biometrics) が提案した手法で、現行試験のパラメータ θ と過去試験のパラメータ θ₀ を「commensurability(適合度)パラメータ τ」で連結します。具体的には θ | θ₀, τ ~ N(θ₀, 1/τ) のように precision τ でborrowing量を決め、τ にも事前分布を置きます。データが整合していれば τ が大きく推定されborrowingが強まり、乖離していれば τ が小さくborrowingが弱まる、という適応的な挙動が特徴です。実装は bayesCT 等で対応します。
| MAP prior | Power Prior | Commensurate Prior | |
|---|---|---|---|
| borrowingの仕組み | 階層モデルの予測分布 | 過去尤度を a₀ 乗で割引 | θ と θ₀ を precision τ で連結 |
| heterogeneity対応 | τ² で自動吸収 | 固定a₀は非対応/NPPは対応 | τ で自動調整 |
| 必要パラメータ | μ, τ²(+ hyperprior) | a₀(固定 or Beta事前) | τ(+ hyperprior) |
| 実装パッケージ | RBesT | NPP, rstanarm | bayesCT |
Borrowingの安全装置:Prior-data conflictとRMAPによる頑健化
過去データを借用する以上、避けて通れないのが prior-data conflict(事前-データ乖離)の問題です。これは「観察された現データが、過去データから構築した事前分布の予測範囲から大きく外れている」状態を指します。例えば過去試験の対照群event rateが10%前後だったのに、現試験では25%が観察された、というケースです。何の安全装置もないとborrowingが裏目に出て、偏ったposteriorで誤った意思決定をしてしまいます。
Prior-data conflictの検出
代表的な検出手法は2つです。1つ目は Box’s prior-data conflict p-value(Box, 1980)で、事前予測分布のもとで観察データがどの程度「裾」に位置するかをp値化します。2つ目は posterior predictive check で、posteriorからレプリカデータを生成し観察値との乖離を視覚化します。FDAガイダンスでは、conflict検出を試験開始前にプロトコルで規定することが推奨されています。
Robust MAP(RMAP)による頑健化
Schmidli et al. (2014, Biometrics) が提案した Robust MAP(RMAP)は、MAP事前分布に「弱情報事前分布(weakly informative prior)」を混合することでconflict時の頑健性を確保します。重み ω ∈ [0, 1] で次のように定義されます。
\[ \pi_{\text{RMAP}}(\theta) = (1-\omega) \cdot \pi_{\text{MAP}}(\theta) + \omega \cdot \pi_{\text{weak}}(\theta) \]
直感としては「ふだんはMAPを (1-ω) の重みで信頼しつつ、もし現データがMAPと乖離していたら、混合分布の性質上 weak成分の重みが後方的に持ち上がりborrowingが自動的に弱まる」という設計です。ωの典型値は 0.1〜0.5 で、FDAガイダンスは ω を試験計画段階で pre-specify することと、感度分析として ω = 0.1, 0.3, 0.5 の3水準で結果を確認することを推奨しています。
RBesTによる実装例
架空の過去6試験(対照群event rate)からMAP事前分布を構築し、robustify を適用するコード例を示します。
library(RBesT)
# 過去6試験の対照群データ(n: 症例数, r: イベント数)
hist_data <- data.frame(
study = paste0("H", 1:6),
n = c(120, 95, 140, 110, 88, 132),
r = c(14, 11, 18, 12, 9, 17)
)
# MAP事前分布の構築(二項モデル、試験間SDに半正規事前)
set.seed(2026)
map_mc <- gMAP(cbind(r, n - r) ~ 1 | study,
data = hist_data,
family = binomial,
tau.dist = "HalfNormal", tau.prior = 1,
beta.prior = 2)
# 混合正規/Beta近似 → robustify でω=0.3を付与
map_prior <- automixfit(map_mc)
rmap_prior <- robustify(map_prior, weight = 0.3, mean = 0.5)
print(rmap_prior)
Univariate beta mixture
Mixture Components:
comp1 comp2 robust
w 0.7000 0.0000 0.3000
a 18.4521 1.0000 1.0000
b 124.7833 1.0000 1.0000
出力の robust 列が weak成分(Beta(1,1)=一様分布、ω=0.3)、comp1 がMAP由来の情報量の多い成分です。robustify() の主要引数は weight(ω)、mean(weak成分の中心)、分布族(binomialの場合は自動でBeta)です。感度分析では weight = 0.1, 0.3, 0.5 でループを回し、posteriorの平均・95%信用区間・borrow有効サンプルサイズ(ess() 関数)の変化を表にまとめると、FDAレビュー対応の説得力が高まります。
Operating Characteristicsの計算:Bayesian Power(Assurance)・Type I Error・MSE
FDA 2026年ドラフトガイダンスが事前分布の妥当性と並んで強く要求しているのが、Operating Characteristics(OC:運用特性)のpre-specified simulationです。ベイズ流の解析であっても、規制当局は試験全体としての頻度論的な振る舞い、特にType I error率を厳格に評価することを求めており、この点は2010年版ガイダンスから一貫しているものの、2026年ドラフトではborrowingを用いる場合のキャリブレーション手順がより明示的になりました。
ガイダンスが要求する主要なOC指標は次の5つです。
- Bayesian power(Assurance):事前分布で重み付けされた頻度論的検出力の期待値。固定の真値ではなく、事前分布上での平均的な成功確率を表します。
- Type I error率:帰無仮説下(θ = θ₀)で誤って有効と結論する確率。borrowingにより膨張しやすい指標です。
- Expected bias:事後平均推定量 E[θ̂ − θ] の真値θに関する期待値。
- Expected MSE:E[(θ̂ − θ)²] の真値上での期待値。borrowingが効くと小さくなりますが、prior-data conflict時には膨らみます。
- Credible interval coverage:95%信用区間が真値を含む頻度論的被覆率。名目水準を大きく外れないことが推奨されます。
Bayesian power(Assurance)は O’Hagan, Stevens, Campbell (2005, Pharmaceutical Statistics) で体系化された概念で、次式で定義されます。
\[ \mathrm{Assurance} = \int \mathrm{Power}(\theta) \, \pi(\theta) \, d\theta \]
ここで Power(θ) は真値θにおける頻度論的検出力、π(θ) は設計時事前分布です。固定の代替仮説のみで検出力を語る従来型と異なり、不確実性そのものを織り込んだ「期待される成功確率」として、近年は意思決定指標として広く用いられています。
もっとも実務上の最大の論点は、borrowingを取り入れた事前分布のもとでType I errorが膨らみうる点です。過去対照データと現在試験の対照群が一致している(prior-data consistency)状況では問題ありませんが、両者にズレ(prior-data conflict)があると、誤った方向にborrowが効いて偽陽性を生みます。FDAは、こうした場合のキャリブレーション手順として、(1) 帰無仮説近傍の複数のθ₀′を含むグリッドでシミュレーションを実施し、(2) 最悪ケースのType I errorが事前指定した上限(典型的に片側0.025)を超えないように、決定閾値や事前分布の robustification weight を調整することを推奨しています。
| OC指標 | 制御する対象 | FDA推奨水準(典型) |
|---|---|---|
| Type I error率 | 偽陽性リスク | 片側 ≤ 0.025(厳守) |
| Bayesian power(Assurance) | 期待成功確率 | ≥ 0.80(設計目標) |
| Expected bias | 推定の偏り | |bias| / SE ≤ 0.25 目安 |
| Expected MSE | 推定精度 | 非借用デザイン比で改善を示す |
| 95% CrI coverage | 区間推定の妥当性 | 0.90〜0.95(名目近傍) |
シミュレーションで運用特性を検証する:R実装ガイド
ここからは、Novartisが公開している RBesT パッケージを用いて、MAP prior/Robust MAP(RMAP)/非借用デザインのOCを比較するシミュレーションを実装します。シナリオは、過去の対照群試験4本(合計N≈400)から MAP prior を構築し、現在試験の対照群サンプルサイズを通常N=80からN=40に削減してborrowing効果を確かめる設定です。
📚 より深く学ぶなら:ベイズ事前分布の構築と臨床試験への応用は専門書での体系学習がおすすめです。記事末の書籍紹介で実務向けの参考書を厳選しました。
# --- パッケージ読み込み ---
library(RBesT) # MAP prior / robustify / OC評価
library(dplyr) # 結果整形
set.seed(20260514) # 再現性確保
# --- 過去対照データ(4試験、応答率と例数) ---
hist <- data.frame(
study = paste0("H", 1:4),
r = c(22, 30, 18, 26), # 奏効数
n = c(100, 120, 80, 100) # 例数
)
# --- MAP prior の構築(半正規ハイパー事前分布でτを制御) ---
map_mc <- gMAP(
cbind(r, n - r) ~ 1 | study,
data = hist,
family = binomial,
tau.dist = "HalfNormal",
tau.prior = 0.5, # 中程度のheterogeneity想定
beta.prior = 2
)
map_prior <- automixfit(map_mc) # 混合β近似
ess_map <- ess(map_prior) # 事前情報量(ESS)
# --- Robust MAP:weakly informative成分を ω=0.2 で混合 ---
rmap_prior <- robustify(map_prior, weight = 0.2, mean = 0.5)
# --- 現在試験設定:対照N=40、治療N=80、真の対照奏効率θ_cで動かす ---
theta_grid <- seq(0.15, 0.35, by = 0.05) # 0.25が過去平均
n_ctrl <- 40
n_trt <- 80
theta_trt_null <- function(tc) tc # H0: 差なし
theta_trt_alt <- function(tc) tc + 0.12 # H1: +12pt
sim_one <- function(prior_ctrl, theta_c, theta_t, N = 10000) {
r_c <- rbinom(N, n_ctrl, theta_c)
r_t <- rbinom(N, n_trt, theta_t)
post_t <- postmix(mixbeta(c(1, 0.5, 0.5)), r = r_t, n = n_trt)
post_c <- lapply(seq_len(N), function(i)
postmix(prior_ctrl, r = r_c[i], n = n_ctrl))
prob <- sapply(seq_len(N), function(i)
pmixdiff(post_t, post_c[[i]], 0, lower.tail = FALSE))
mean(prob > 0.975)
}
# --- 各シナリオで Type I error と Power を計算 ---
res <- expand.grid(prior = c("RMAP", "MAP", "None"), theta_c = theta_grid) %>%
rowwise() %>%
mutate(
prior_obj = list(switch(prior,
RMAP = rmap_prior,
MAP = map_prior,
None = mixbeta(c(1, 0.5, 0.5)))),
T1E = sim_one(prior_obj, theta_c, theta_trt_null(theta_c)),
Power = sim_one(prior_obj, theta_c, theta_trt_alt(theta_c))
) %>% select(-prior_obj)
print(as.data.frame(res))
cat("MAP prior ESS:", round(ess_map, 1), "\n")
典型的な出力例(架空の代表値)は次のようになります。過去平均θ_c = 0.25 近傍ではRMAP/MAPともにType I errorは0.025前後に収まり、N=40でも非借用N=80相当のPowerを再現できる一方、θ_c = 0.35 のprior-data conflictシナリオではMAPのType I errorが0.075まで膨らみ、RMAPは0.035に抑制されることが確認できます(MAP prior ESS ≈ 38)。
# prior theta_c T1E Power
# RMAP 0.15 0.028 0.812
# MAP 0.15 0.061 0.835
# None 0.15 0.024 0.703
# RMAP 0.25 0.022 0.851
# MAP 0.25 0.021 0.882
# None 0.25 0.025 0.704
# RMAP 0.35 0.035 0.798
# MAP 0.35 0.075 0.760 # ← T1E膨張
# None 0.35 0.024 0.706
結論として、borrowing量(実質ESS)が大きいほどprior-data conflict時のType I error膨張が顕著になり、Robust成分の重みωを0.1〜0.3の範囲でsensitivity analysisを行い、最悪ケースのType I errorが片側0.025を逸脱しない設定を選ぶことが、規制対話における推奨アプローチです。
規制対話に向けた事前パッケージ:ガイダンスが求めるドキュメント要件
本ガイダンスがもっとも強く打ち出しているメッセージのひとつが、「ベイズ流アプローチを採用する場合は、可能なかぎり早期にFDAと対話せよ」という点です。具体的にはPre-IND meetingやType B meetingの段階で、統計デザインの骨子を当局と共有し、合意形成を進めることが推奨されています。試験開始後に手法をめぐって紛糾するリスクを下げ、レビューの予見可能性を高めるための実務的な配慮といえます。
規制対話の場でスポンサーが用意すべきドキュメントは、ガイダンスの記述および過去のType B meeting実務を踏まえると、おおむね次の要素に整理できます。
- シミュレーションレポート(Simulation Report):想定する事前分布・治療効果・症例数のもとで、Bayesian powerおよび頻度論的Type I errorを評価したレポート。シナリオは帰無仮説下と複数の対立仮説下を網羅し、各シナリオの試行回数(通常10,000回以上)を明示します。
- 事前分布の正当化文書(Prior Justification):情報事前分布を使う場合、その根拠データ(過去試験、文献、専門家エリシテーション)と、有効サンプルサイズ(ESS:Effective Sample Size)による事前情報量の定量評価を含めます。
- 感度分析(Sensitivity Analyses):事前分布のパラメータを変動させたときの結論の頑健性を、複数のtipping point分析や代替事前分布で確認した結果。
- Prior-data conflict対応策:観測データが事前分布と乖離した場合の取り扱いを事前に規定。具体的にはCommensurate priorやrobust mixture prior(RMAP)を採用するのか、動的borrowingで重みを自動調整するのかを明記します。
- 解析計画書(SAP)のベイズ流補遺:事後分布の要約方法、判定基準(例:事後確率>0.975)、欠測データの取り扱い、中間解析がある場合のα消費の代替指標などを記述します。
これらのドキュメントは、Briefing bookの統計セクションとして統合され、Meeting requestと同時に提出されます。Briefing bookには、議論したい論点(Question)を明確にし、スポンサー側の見解(Sponsor’s Position)を添える形式が一般的です。「事前分布の選択は妥当か」「シミュレーションのシナリオ網羅性は十分か」「Type I errorの制御水準は受け入れ可能か」といった論点を具体化することで、当局からのフィードバックが得られやすくなります。
実務での落とし穴と推奨アプローチ
ここまでの実装を踏まえ、規制申請を見据えたベイズデザインで実務者が陥りやすい落とし穴を5点に整理します。いずれもFDAアドバイザリー・コミッティーや Type C meeting で頻繁に指摘されるポイントです。
- 事前分布をpre-specifyしない:プロトコル/SAPで事前分布の具体形(混合成分・ハイパーパラメータ・ω)を確定せず、データを見てから調整するのは2026年ドラフトが最も警戒する違反パターンです。事前分布はlocked SAPに数式と数値で記載し、変更履歴を追跡可能にしてください。
- 過去試験のheterogeneityを過小評価:τ²(試験間分散)の事前分布をHalfNormal(0, 0.125)のように過度にタイトに置くと、見かけ上ESSが膨らんで申請時に却下されます。HalfNormal(0, 0.5)以上を起点に、τの事前分布感度分析を必ず添付すべきです。
- Operating characteristicsをsimulation報告書で省略:Type I error・Power・bias・MSE・CrI coverageの5指標を、真値グリッド全体について表とプロットで提示しない申請は、ほぼ確実に追加情報要求(Information Request)の対象になります。
- Robust mixture weight ω のsensitivity analysisを実施しない:ω=0.2固定で報告するだけでは不十分で、ω∈{0.1, 0.2, 0.3, 0.5}でType I error・Powerがどう動くかを示し、選択根拠を文章化することが推奨されます。
- Borrowingの上限ESSを事前に公表しない:「現在試験の対照群nに対してESSは最大n/2まで」など、borrowingの上限をプロトコルに明記しないと、データ依存的にborrowが暴走したと受け取られます。ESS capをルール化し、SAPで宣言してください。
これら5点は単独のテクニカル問題ではなく、「事前にすべて宣言し、シミュレーションで裏付ける」というガイダンス全体の哲学を実装レベルに落としたものです。逆に言えば、この5項目をチェックリスト化して開発初期から運用すれば、規制対話の8割は既に勝負がついていると言えます。
まとめ
2026年1月に公開されたFDAベイズドラフトガイダンスは、医薬品・生物製剤領域におけるベイズ流アプローチの位置づけを大きく前進させる文書です。事前分布の正当化、外部情報のBorrowing、Operating Characteristicsの評価、シミュレーションによる事前キャリブレーション、そして規制との早期対話という五つの柱が、実務的なフレームワークとして提示されています。とくに、Bayesian powerとType I errorを併記する評価方針、Prior-data conflictへの備え、Briefing bookへの統計セクション充実といった点は、今後の確証的試験のデザインに直接影響を与えるでしょう。スポンサー側の生物統計担当者は、シミュレーション基盤と事前分布の正当化資料を整備し、Pre-INDの段階から規制対話を主導していく姿勢が求められます。
ベイズ流の基礎やFDAガイダンス概要は「ベイズ臨床試験デザイン入門 ─ FDA 2026年ドラフトガイダンスから読み解く事前分布・予測確率・適応的デザイン」で扱っています。製薬業界での活用例は「ベイズ統計の解析手法と製薬業界での活用 ─ RとSAS」、外部対照群とベイズ動的借用の関係については「外部対照群の統計手法(2/2) ─ 傾向スコアマッチング・MAIC・ベイズ動的借用」、アダプティブデザインの規制動向については「ICH E20(臨床試験のためのアダプティブデザイン)とは」で詳しく解説しています。
📚 この記事をより深く理解するための参考書籍
FDAベイズドラフトガイダンスを実務に落とし込むには、Stan・Rでの実装力と事前分布の数理的直観の両方が必要です。下記の3冊は当ブログで未紹介の和書から、本記事の読者層(生物統計実務者・規制対応担当)が次の一歩を踏み出すために厳選しました。